
氯化铵和氯化钠可用下列哪一种方法分离
A.加入氢氧化钠 B.加入AgNO3溶液 C.加热法 D.加入一种合适的酸 E.加入水
C
物质的分离不同于鉴别,鉴别是采取一定的方法,能将两种或几种物质分辨出来就可。而分离是将几种成分采取一定的措施分离成各单一的成分。
分离可根据物理性质用物理分法进行分离,比如根据各组分的溶解性不同,用过滤的方法分离;根据各组分的沸点不同,用蒸馏的方法分离;根据各组分在同一溶剂中的溶解度不同用结晶的方法分离。也可根据各组分的化学性质不同,加入某些试剂,采取一定方法进行分离。
根据以上分析,题目所给NaCl和NH4Cl只能用化学方法分离,因为两种物质中都含Cl-,所以加AgNO3或加酸都起不到分离的作用,加入NaOH,只能鉴别NH4Cl和NaCl,而达不到分离的目的。两种物质又均易溶于水,因此加入水也无法分离。那么方法只有一种,利用铵盐的不稳定,及NH3的化学性质,所以选用加热法。


科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸氢铵 | 15.8 | 21.0 | 27.0 | 分解 |
| 碳酸氢钠 | 8.1 | 9.6 | 11.1 | 12.7 |
| 氯化铵 | 33.3 | 37.2 | 41.4 | 45.8 |
查看答案和解析>>
科目:高中化学 来源:广东省2009届高三化学各地名校月考试题汇编-碱金属 题型:058
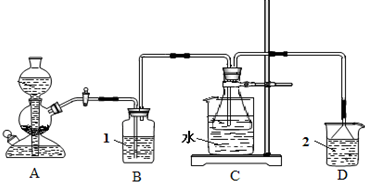
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O![]() NH4Cl+NaHCO3↓依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
NH4Cl+NaHCO3↓依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
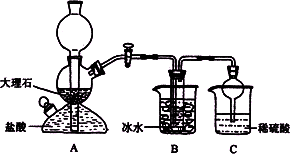
(1)A装置中所发生反应的离子方程式为:________.
C装置中稀硫酸的作用为:____________________.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100 g水)

参照表中数据,请分析B装置中使用冰水是因为________.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在________装置之间(填写字母)连接一个盛有________的洗气装置,其作用是________.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85 g,实验后得到干燥的NaHCO3晶体的质量为5.04 g,则NaHCO3的产率为________.
查看答案和解析>>
科目:高中化学 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:
NH3+CO2+NaCl+H2O![]() NH4Cl+NaHCO3↓依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
NH4Cl+NaHCO3↓依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
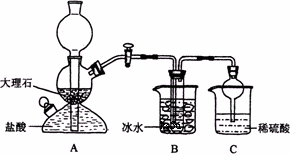
(1)A装置中所发生反应的离子方程式为:________.
C装置中稀硫酸的作用为:________.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100 g水)
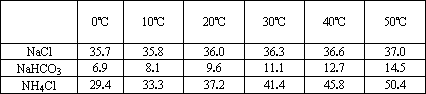
参照表中数据,请分析B装置中使用冰水是因为________.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在________装置之间(填写字母)连接一个盛有________的洗气装置,其作用是________.
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85 g,实验后得到干燥的NaHCO3晶体的质量为5.04 g,则NaHCO3的产率为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3+CO2+NaCl+H2O====NH4Cl+NaHCO3(晶体)
依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:

(1)A装置中所发生反应的离子方程式为_____________,C装置中稀硫酸的作用为_________________________。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/l00g水)
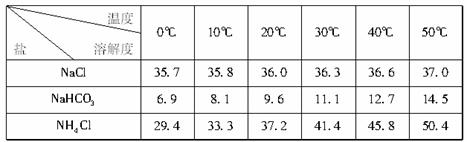
参照表中数据,请分析B装置中使用冰水是因为__________________________________。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在_____________装置之间(填写字母)连接一个盛有____________的洗气装置,其作用是_________________________________________________________________.
(4)利用改进后的装置进行实验,在B中的试管中析出了晶体,经必要的操作后得到了一种纯净的晶体。现有下列试剂:盐酸、浓氨水、生石灰、蒸馏水,利用本题所提供的试剂(只限一种)及试管、酒精灯等主要仪器,通过简单实验判断该晶体是碳酸氢钠晶体,而不是碳酸氢铵或食盐晶体,简述操作方法、实验现象及结论:_________________________________________。
(5)若该校学生进行实验时,所用饱和食盐中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O NH4Cl+NaHCO3(晶体)依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
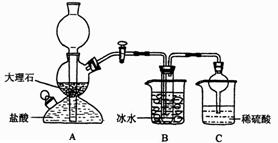
(1)A装置中所发生反应的离子方程式为 。
C装置中稀硫酸的作用为 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)

参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体。现有下列试剂:盐酸、浓氨水、生石灰、蒸馏水,利用本题所提供的试剂(只限一种)及试管、酒精灯等主要仪器,通过简单实验判断该晶体是碳酸氢钠晶体,而不是碳酸氢铵或食盐晶体,简述操作方法、实验现象及结论:
。
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com