
分析 (1)在水溶液里或熔融状态下导电的化合物是电解质,包括:酸、碱、盐、金属氧化物、水;
在水溶液和熔融状态下都不导电的化合物是非电解质,包括大多是有机物、非金属氧化物、氨气;
(2)硝酸铵的化学式是 NH4NO3,氨气的化学式是NH3.
解答 解:(1)①Fe是单质,既不是电解质,也不是非电解质;
②CO2是非金属氧化物,属于非电解质;
③Cu(OH)2是碱,属于电解质;
④C2H5OH(酒精)水溶液和熔融状态下都不导电的化合物,属于非电解质;
⑤MgCl2溶液为混合物,既不是电解质,也不是非电解质;
⑥硝酸铵属于盐,是电解质;
⑦氨气,属于非电解质;
⑧NaCl固体,属于电解质;
所以属于电解质的有:③⑥⑧;属于非电解质的有:②④⑦;
故答案为:③⑥⑧;②④⑦;
(2)硝酸铵的化学式是 NH4NO3,氨气的化学式是NH3,故答案为:NH4NO3;NH3.
点评 本题考查了电解质和非电解质的判断,明确二者的概念和区别是解本题关键,注意单质和混合物既不是电解质也不是非电解质,为易错点.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
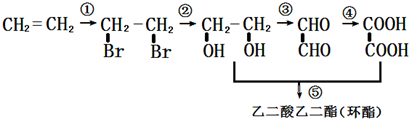
 ;
; +H2O,;
+H2O,; .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验内容 | 现象或结论 |
| A | 向2SO2+O2?2SO3的平衡体系中加入由18O构成的氧气 | 则SO2中的18O的含量会增加 |
| B | 以石墨为电极,电解KI溶液(其中含有少量酚酞) | 阴极逸出气体且附近溶液呈现红色 |
| C | FeCl3+3KSCN?Fe(SCN)3+3KCl 平衡体系中加入少量KSCN固体,溶液颜色加深 | 恒温时增大反应物浓度,平衡向正反应方向移动 |
| D | 向pH=1的盐酸和醋酸各0.5L的溶液中各加入1.4g铁粉 | 醋酸中生成H2的速率快且最终气体量多 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com