
(15��)
I2O5�ǰ�ɫ���壬��ˮ���ɵ��ᣨHIO3����I2O5�����ڼ��鲢�����ⶨ�����е�CO���ڳ����·����ķ�ӦΪ 5CO��I2O5=5CO2��I2���������������岻��I2O5��Ӧ����
ʵ��һ����ȡI2O5
�����������90~110 ?Cʹ�䲿����ˮ����������220~240 �沢����4 h��ʹ��Ӧ��ȫ������������ȴ�����£��ܷⱣ�棬�������������⡣
��1��д��������I2O5�Ļ�ѧ����ʽ�� ��
��2�����Ƶõ�I2O5�����к�������I2���ʣ��ᴿ�ķ����� �����ţ���
A������ B�������ᾧ C������ D������
���ᴿ�����õ��IJ�������Ϊ �����ţ���
A��Բ����ƿ B���ձ� C����ͨ©�� D���ƾ��� E��������
ʵ��������������CO������ͼװ�ü���������Ƿ����CO��
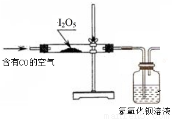
��3����˵�������к���CO�������� ��
��4������Ҫ�ӹ��ƿ�г��ֻ������жϿ����к���CO����д���Ľ���ʵ�鷽���� ��
ʵ�������ⶨ������CO�ĺ���
��5����I2O5��CO��Ӧ���ɵĵⵥ������������Ƶζ�����ӦΪI2��2Na2S2O3=Na2S4O6��2NaI�������ɸ���������������Ƶ��������������CO�ĺ�������ij��ʵ��ʱ��ò��뷴Ӧ�Ŀ������Ϊa mL����״���£����ζ������У�������v mL c mol��L-1 Na2S2O3��Һ����ÿ�����Ʒ��CO����������� ��
��6����ʵ�鷽�����ڵ�һ������ȱ���� ��
(15��)
��1��2HIO3 I2O5��H2O��3�֣�
I2O5��H2O��3�֣�
��2��D (2��) A B D��2�֣�
��3���������а�ɫ�����Ϊ�Ϻ�ɫ��2�֣�
��4����������Ӳ�ʲ�����֮ǰ��������ͨ��װ������������Һ��Ũ�����ϴ��ƿ��2�֣�
��5�� 56cv/a��2�֣�
��6��ȱ��ƽ��ʵ�� ��2�֣�
��������
�����������1�����ȵ���ֽ������I2O5��H2O�����Ի�ѧ����ʽΪ��2HIO3 I2O5��H2O��
I2O5��H2O��
��2���������������Կ�ͨ�������ķ���I2O5�����к�������I2���ʣ�������Ҫ�õ��������У��ƾ��ơ���ƿ�������������Դ�ΪABD��
��3��������Ŀ������Ϣ���ڳ����·����ķ�ӦΪ 5CO��I2O5=5CO2��I2 ���������������岻��I2O5��Ӧ�����������к���CO�����ɵ�I2Ϊ�Ϻ�ɫ��������˵�������к���CO�������ǣ��������а�ɫ�����Ϊ�Ϻ�ɫ��
��4������Ҫ�ӹ��ƿ�г��ֻ������жϿ����к���CO��Ϊ�˷�ֹ������CO2�ĸ��ţ�ͨ������������Һ��ȥ�����е�CO2��Ϊ�˷�ֹI2O5��ˮ��Ӧ����ҪŨ���������ԸĽ���ʵ�鷽��Ϊ����������Ӳ�ʲ�����֮ǰ��������ͨ��װ������������Һ��Ũ�����ϴ��ƿ��
��5�����ݻ�ѧ����ʽ�ɵö�Ӧ��ϵ��5CO �� I2 ��2Na2S2O3 ����n��CO��=5/2n��Na2S2O3��=5/2��vc/1000mol�����Ըÿ�����Ʒ��CO���������=5/2��vc/1000mol��22.4L/mol��a/1000L=56cv/a��
��6������ÿһ��ʵ�鶼��żȻ�ԣ�Ϊ��ʹ�ⶨ��ֵ�ӽ���ʵֵ��Ӧ�ü������ʵ�飬��ƽ��ֵ�����Ը�ʵ�鷽�����ڵ�һ������ȱ���ǣ�ȱ��ƽ��ʵ�顣
���㣺���⿼�黯ѧ����ʽ����д�����������ͻ���������ʵ�鷽������������ۡ���ѧ���㡣


 ���Ǽ���С����ϵ�д�
���Ǽ���С����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ����Ϫһ�и�����ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���һ�����������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬�õ�200 mL c(OH-)= 0.1mol/L����Һ��Ȼ����μ���1 mol/L �����ᣬ������ɳ���������m��������������V��ϵ��ͼ��ʾ��

������˵����ȷ����
A��ԭ�Ͻ�����Ϊ 0.92 g
B��ͼ��V2Ϊ 100
C������������������� Na����Ũ�ȱ��ֲ���
D��Q��m1Ϊ0.78
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ����Ϫ��һ��ѧ����9�������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A��48gO3���庬��6.02��1023��O3����
B��5.6g Fe��������ϡ���ᷴӦת�Ƶ���0.3 mol
C��0.5mol��L-1CuCl2��Һ�к���3.01��1023��Cu2+
D����״���£�33.6LH2O����9.03��1023��H2O����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ������������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��HF��HCl��HBr��HI�����ȶ������μ������е�ȴ��������
B������״̬���ܵ���Ļ�����һ�������Ӽ���������ǽ���Ԫ���γɵĻ�����һ�������ӻ�����
C��NaHSO4���������������ӵĸ�����1��2���ۻ�ʱ�ƻ��������Ӽ����ۼ�
D��NCl3���������е�ԭ�Ӿ�Ϊ8�����ȶ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ������������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й������л�ѧ�������������
A����ȼ��ú�м�����ʯ�ң����Լ��ٶԴ�������Ⱦ
B����˫��ˮ��ϴ�˿ڣ�����ɱ������
C��ֻ�õ�����Һ���ܼ����ʳ�����Ƿ�ӵ�
D�����ⶪ���Ͼɵ�أ���Ի��������Ⱦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��ѧ�̲��У���������ͼ�����һ�����ֶ�������ͻ��ʵ��װ�õ�Ҫ�㡢����ز�����ѧ���̵�ԭ���������йػ�ѧͼ����ֵ�������ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ�ڰ��ڿ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��w�������ʵ�ת����ϵ��ͼ��ʾ�����ַ�Ӧ��Ͳ����Ѿ�ʡ�ԣ���

��������в����ϸù�ϵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�ĵ���У������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���з�Ӧ�����ӷ�Ӧ����ʽΪ
A������ʯ���ڴ�����Һ�� CaCO3 + 2H+==Ca2+ + CO2��+ H2O
B����FeBr2��Һ��ͨ������������2Fe2+ + 4Br- + 3Cl2=== 2Fe3+ + 2Br2 + 6Cl-
C��NH4HCO3���ڹ�����NaOH��Һ�У�HCO3- + OH- === CO32- + H2O
D����������KAl(SO4)2��12H2O����Һ�еμ�Ba(OH)2��Һ��ǡ��ʹSO42-������ȫ��
2Al3+ + 3SO42- + 3Ba2+ + 6OH-=== 2Al(OH)3�� + 3BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�߶���ѧ�ڰ���������ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ�����缫�Ϸ����ĵ缫��Ӧ���£�a����2H����2e��===H2����b����Cu��2e��== Cu 2��

����˵������ȷ����
A��X��Һ��pH����
B����װ�ÿ����ǽ���ѧ��ת��Ϊ����
C����װ��һ���ǵ���
D��a��b������ͬ�ֵ缫����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com