
【题目】氮的固定意义重大,氮肥的大面积使用提高了粮食产量。
(1)目前人工固氮有效且有意义的方法是_______________(用一个化学方程式表示)。
(2)自然界发生的一个固氮反应是N2(B)+O2(g) ![]() 2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ·mol-1、498kJ·mol-1、632kJ·mol-1,则该反应的△H=____kJ·mol-1。
2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ·mol-1、498kJ·mol-1、632kJ·mol-1,则该反应的△H=____kJ·mol-1。
(3)恒压100kPa时,反应2NO(g)+O2(g)![]() 2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)
2NO2(g)中NO的平衡转化率与温度的关系曲线如图1,反应2NO2(g)![]() N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。
N2O4(g)中NO2的平衡转化率与温度的关系曲线如图2。
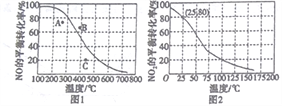
①图1中A、B、C三点表示不同温度、压强下2NO(g)+O2(g)![]() 2NO2(g)达到平衡时NO的转化率,则____________点对应的压强最大。
2NO2(g)达到平衡时NO的转化率,则____________点对应的压强最大。
②恒压100kPa、25℃时,2NO2(g) ![]() N2O4(g)平衡体系中N2O4的物质的量分数为______________,列式计算平衡常数Kp=____________。(Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
N2O4(g)平衡体系中N2O4的物质的量分数为______________,列式计算平衡常数Kp=____________。(Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)室温下,用往射器吸入一定量NO2气体,将针头插入胶塞密封,然后迅速将气体体积压缩为原来的一半并使活塞固定,此时手握针筒有热感,继续放置一段时间。从活塞固定时开始观察,气体颜色逐渐__________(填“变深”或“变浅”),原因是________________。[已知2NO2(g)![]() N2O4(g)在几微秒内即可达到化学平衡]
N2O4(g)在几微秒内即可达到化学平衡]
【答案】 N2+3H2![]() 2NH3 +180 B 66.7% (100KPa/66.7%)/[100KPa/(1-66.7%]2 变浅 活塞固定时2NO2(g)
2NH3 +180 B 66.7% (100KPa/66.7%)/[100KPa/(1-66.7%]2 变浅 活塞固定时2NO2(g) ![]() N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低
【解析】分析:(1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨;(2)热化学方程式中,反应焓变=反应物的总键能-生成物的总键能,据此计算;(3)①2NO(g)+O2(g)![]() 2NO2(g),反应是气体体积减小的反应压强越大平衡正向进行,图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa;②利用三段法列式计算,恒压100kPa、25
2NO2(g),反应是气体体积减小的反应压强越大平衡正向进行,图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa;②利用三段法列式计算,恒压100kPa、25![]() 时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g) ![]() N2O4(g)
N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=![]() ×100%=66.7%,
×100%=66.7%,
Kp用平衡分压代替平衡浓度计算,分压=总压×物质的量分数列式计算;
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g) ![]() N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动, NO2浓度降低,颜色变浅。
N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动, NO2浓度降低,颜色变浅。
详解:(1)游离态的氮元素反应生成化合态氮元素为氮的固定,如工业合成氨,反应的化学方程式为: N2+3H2![]() 2NH3,因此,本题正确答案是: N2+3H2
2NH3,因此,本题正确答案是: N2+3H2![]() 2NH3;
2NH3;
(2) N2(B)+O2(g) ![]() 2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ·mol-1、498kJ·mol-1、632kJ·mol-1,则该反应的△H=(946kJ·mol-1+498kJ·mol-1)-2×632kJ·mol-1=+180kJ·mol-1,因此,本题正确答案是:+180;
2NO(g),已知N2、O2、NO三种分子中化学键断裂所吸收的能量依次为946kJ·mol-1、498kJ·mol-1、632kJ·mol-1,则该反应的△H=(946kJ·mol-1+498kJ·mol-1)-2×632kJ·mol-1=+180kJ·mol-1,因此,本题正确答案是:+180;
(3)①图中曲线上各点为等压不等温,通过控制变量做等温线确定ABC三点与曲线交点等温不等压,从而确定曲线以下的点压强小于100kPa,曲线以上的点压强大于100kPa,所以B点压强最大,因此,本题正确答案是:B;
②25![]() 时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
时NO2的转化率为80%,设起始量二氧化氮物质的量为x,
2NO2(g) ![]() N2O4(g)
N2O4(g)
起始量(mol) x 0
变化量(mol) 0.8x 0.4x
平衡量(mol) 0.2x 0.4x
平衡体系中N2O4的物质的量分数=![]() ×100%=66.7%,
×100%=66.7%,
Kp用平衡分压代替平衡浓度计算,分压=总压![]() 物质的量分数,
物质的量分数,
则Kp=(100KPa/66.7%)/[100KPa/(1-66.7%]2
因此,本题正确答案是: 66.7% ;(100KPa/66.7%)/[100KPa/(1-66.7%]2 。
(4)压缩活塞平衡正移,反应放热,针管微热,活塞固定时2NO2(g) ![]() N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅。
N2O4(g)已达平衡状态,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低,颜色变浅。
因此,本题正确答案是:变浅;活塞固定时2NO2(g) ![]() N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低。
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低。


科目:高中化学 来源: 题型:
【题目】铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
(氯化铁)熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
(氯化亚铁)熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
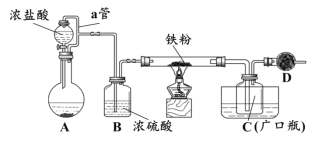
(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为_________。仪器D的名称是__________________。
(2)D中装的药品是碱石灰,其作用是__________________________。
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的_____(只能选取一种试剂,填序号)进行检测,实验现象是__________________________________。
①H2O2 溶液 ②KI-淀粉溶液 ③KSCN溶液 ④酸性KMnO4溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。
则该样品中铁元素的质量分数为_______%(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施。
①用题目所给的装置制得的产物中,铁元素含量______(填“相等”、“偏高”或“偏低”),说明含有FeCl2杂质。
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出了“积极参与全球环境治理,落实减排承诺”。其中氮的化合物的处理和利用是环境科学研究的热点。
(1)机动车排放的尾气中主要污染物为NOx ,可用 CH4 催化还原 NOx 以消除其污染。298 K时,1.0 g CH4 (g)与足量的NO气体完全反应生成N2、CO2和H2O(g),放出72. 5 kJ的热量。该反应的热化学方程式为_______________。
(2)氮氧化物与悬浮大气中的海盐粒子相互作用会生成NOCl,涉及的相关反应有:
热化学方程式 | 平衡常数 | |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
ΔH1、ΔH2、ΔH3之间的关系为ΔH3=___________;K1、K2、K3的关系为K3=____________。
(3)对汽车加装尾气净化装置,可使汽车尾气中含有的CO、NO2等有毒气体转化为无毒气体:4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1。对于该反应,温度不同(T2﹥T1),其他条件相同时,下列图像正确的是________(填序号)。
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1。对于该反应,温度不同(T2﹥T1),其他条件相同时,下列图像正确的是________(填序号)。
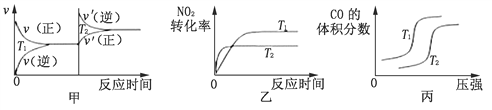
(4)用活性炭还原法也可以处理氮氧化物。向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s) +2NO(g)![]() N2(g) + CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g) + CO2(g) ΔH。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
① T1℃时,该反应在0~20min的平均反应速率v(CO2)=__________________;该反应的平衡常数K= _____________;
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_______(填序号);
A. 加入一定量的活性炭 B. 恒温恒压充入氩气
C. 适当缩小容器的体积 D. 加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则和原平衡相比,NO的转化率_____________(填“升高”或“降低”),ΔH_______0(填“﹥”、“﹤”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知K2Cr2O7溶液中存在如下平衡:Cr2O72-(aq,橙色)+H2O(l)![]() 2H+(aq)+2CrO42-(aq,黄色),现进行如下实验:①向试管中加入4mL0.1mol/LK2Cr2O7溶液,再滴加1mol/LNaOH溶液至稍过量;②向①所得溶液中滴加1mol/LHNO3溶液至稍过量。下列分析不正确的是
2H+(aq)+2CrO42-(aq,黄色),现进行如下实验:①向试管中加入4mL0.1mol/LK2Cr2O7溶液,再滴加1mol/LNaOH溶液至稍过量;②向①所得溶液中滴加1mol/LHNO3溶液至稍过量。下列分析不正确的是
A. 上述反应平衡常数的表达式为:K=[c(H+)·c2(CrO42-)]/[c(Cr2O72-)·c(H2O)]
B. 实验①现象:溶液由橙色变为黄色,实验②现象:溶液由黄色变为橙色
C. 实验①和②的目的是探究H+浓度对上述平衡的影响
D. 预测稀释K2Cr2O7溶液时,溶液颜色由橙色变为黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为_____________; lmol O22+中含有的π键数目为_______________。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2红棕色沉淀。Cu+基态核外电子排布式为_________。
(3)乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是___________________;分子中处于同一直线上的原子数目最多为_______________。
(4)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),则该晶胞中的碳原子个数为______。 CaC2晶体中含有的中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2 晶体中1个Ca2+周围距离最近的C22-数目为_________________。
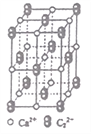
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示,已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,B和D都是日常生活食品中常见的有机物,E是具有浓郁香味、不易溶于水的油状液体,F是一种高聚物,生活中用于制造食物保鲜膜。
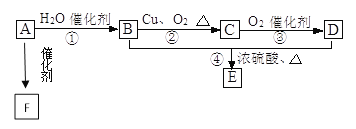
(1)请写出A的结构简式________、C的结构式__________;
(2)请写出B中官能团的电子式__________、D中官能团的名称__________;
(3)请写出下列反应的类型:①__________,②________,④__________。
(4)请写出下列物质转化的化学方程式:A→F ____________; B→C _______;B+D→E __________。
Ⅱ.在实验室可以用如图所示的装置进行B与D的反应,请回答下列问题:
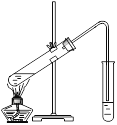
(1)装置中通蒸气的导管要插在_______溶液的液面上方,而不能插入溶液中的原因是为了________,该溶液的作用是____________________________________。
(2)若要把制得的乙酸乙酯分离出来,应采用的实验操作是______。
Ⅲ. 苹果醋是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果酸是苹果醋的主要成分,其结构简式如图所示,请回答下列问题:
![]()
(1)苹果酸的分子式为__________。
(2)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气____L。
(3)在一定条件下,苹果酸可能与下列哪些物质发生反应?_________
A.氢氧化钠溶液 B.乙酸 C.碳酸氢钠溶液 D.乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路、陶瓷等生产领域。工业上由氧化铝与焦炭在氮气流中高温制得:Al2O3+3C+N2![]() 2AlN+3CO。请回答:
2AlN+3CO。请回答:
(1)上述反应中氧化剂与还原剂的物质的量之比___________________。
(2)制得的氮化铝产品中常含有Al4C3、Al2O3和C等杂质,已知:
稀硫酸(过量) | 浓NaOH溶液(过量) | |
AlN | 2AlN+4H2SO4=Al2(SO4)3+(NH4)2SO4 | AlN+NaOH+H2O=NaAlO2+NH3 ↑ |
Al4C3 | Al4C3+6H2SO4=2Al2(SO4)3+3CH4 ↑ | Al4C3+4NaOH+4H2O=4NaAlO2+3CH4 ↑ |
为测定产品中AlN和Al4C3的含量,设计了如下两套实验装置(在通风橱进行,可适当微热,忽略空气中水蒸气、CO2的影响及NH3在强碱性溶液中的溶解)。

装置I、II在反应前后的质量差分别为m1 g和m2 g,则m g产品中AlN的质量分数为______(用含m、m1、m2的代数式表示)。
(3)取装置I中反应后的滤液,先加入少量(NH4)2SO4溶液,然后依次进行蒸发浓缩、冷却结晶、过滤、用少量酒精洗涤、滤纸吸干,得到铵明矾晶体[NH4Al(SO4)2·12H2O]。
①蒸发浓缩操作时,除需铁架台(带铁圈)、酒精灯、坩埚钳、玻璃棒外,还需要_______(填仪器名称);蒸发浓缩的操作;小火加热,不断搅拌,_________。
②用少量酒精洗涤的目的__________________________。
(4)已知:25℃时,Kw=1.0×10-14,Kb(NH3·H2O)=1.8×10-5,Kb(Al(OH)3]=1.4×10-9。
① NH4Al(SO4)2溶液中离子浓度由大到小的顺序_________________。
②(NH4)2SO4溶液中存在水解平衡,则水解平衡常数为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不是氧化还原反应的是
A. 3Cl2+6KOH===5KCl+KClO3+3H2O
B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D. 2AgNO3+BaCl2===2AgCl↓+Ba(NO3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com