
| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
分析 (1)若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol,由方程式可知,消耗氮气为0.2mol×$\frac{1}{2}$=0.1mol,消耗氢气为0.2mol×$\frac{3}{2}$=0.3mol,根据v=$\frac{△c}{△t}$计算v(N2),H2的转化率=$\frac{物质的量变化量}{起始物质的量}$×100%;
(2)A.加了催化剂,不影响平衡移动;
B.增大容器体积,压强减小,平衡向气体体积增大方向移动;
C.降低反应体系的温度,平衡向放热反应方向移动;
D.加入一定量N2,平衡正向移动;
(3)①正反应为放热反应,升高温度平衡逆向移动,平衡常数减小;
②可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
③400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数;
计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行;
(4)A.化学反应速率表示反应快慢;
B.根据勒夏特列原理,改变条件使平衡正向移动;
C.使用催化剂不影响平衡移动;
D.化工生产经济效益需要考虑产量及原料利用率.
解答 解:(1)若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol,由方程式可知,消耗氮气为0.2mol×$\frac{1}{2}$=0.1mol,消耗氢气为0.2mol×$\frac{3}{2}$=0.3mol,则v(N2)=$\frac{\frac{0.1mol}{2L}}{5min}$=0.01mol/(L.min),H2的转化率=$\frac{0.3mol}{0.6mol}$×100%=50%,
故答案为:0.01mol/(L.min);50%;
(2)A.加了催化剂加快反应速率,不影响平衡移动,氢气转化率不变,故A错误;
B.增大容器体积,压强减小,平衡向逆反应方向移动,氢气转化率减小,故B错误;
C.正反应为放热反应,降低反应体系的温度,平衡正向移动,氢气转化率增大,故C正确;
D.加入一定量N2,平衡正向移动,氢气转化率增大,故D正确,
故选:CD;
(3)①正反应为放热反应,升高温度平衡逆向移动,平衡常数减小,故K1>K2,
故答案为:>;
②A.平衡时各组分浓度之比与起始浓度及转化率有关,平衡时浓度之比不一定等于化学计量数之比,故A错误;
B.应是v(H2)正=3v(N2)逆时反应到达平衡,故B错误;
C.随反应进行气体物质的量减小,恒温恒容下压强减小,容器内压强保持不变说明反应到达平衡,故C正确;
D.混合气体的总质量不变,容器容积不变,混合气体的密度为定值,故D错误,
故选:C;
③400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数与N2(g)+3H2(g)?2NH3(g)的平衡常数互为倒数,则400℃时,反应2NH3(g)?N2(g)+3H2(g)的化学平衡常数K=$\frac{1}{0.5}$=2;
此时浓度商Qc=$\frac{\frac{2}{2}×(\frac{1}{2})^{3}}{(\frac{3}{2})^{2}}$=$\frac{1}{18}$<K=2,反应向正反应进行,则该反应的v(N2)正>v(N2)逆,
故答案为:2;>;
(4)A.化学反应速率表示反应快慢,可指导怎样在一定时间内快出产品,故A正确;
B.根据勒夏特列原理,改变条件使平衡正向移动,可指导怎样使用有限原料多出产品,故B正确;
C.使用催化剂加快反应速率,一定时间内快出产品,但不影响平衡移动,不能提高产品产率,故C错误;
D.化工生产经济效益需要考虑产量及原料利用率,改变条件,增大化学反应速率,使平衡正向移动,可以提高化工生产的综合经济效益,故D正确;
故选C.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、平衡常数计算及应用、化学反应速率计算与影响因素等,掌握化学平衡常数的用途:1、判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、计算转化率等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | B. | 4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||
| C. | 2F2+2H2O=4HF+O2↑ | D. | 2Na+2H2O=2NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | A | B | C | |||||
| 三 | D | E | F | G |
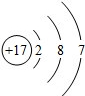 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 35℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 2mol CH3OH | 2mol CH3OH | |
| 平 均 数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | aKJ | bKJ | cKJ | |
| 体系压强 | P1 | P2 | P3 | |
| 反转化率应物 | a1 | a2 | a3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
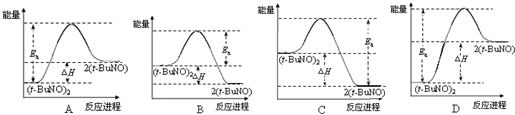
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | C+H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO+H2 | ||
| C. | Cl2+H2O═HCl+HClO | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫常用来漂白纸浆 | B. | 漂粉精可用于游泳池的消毒 | ||
| C. | 明矾常用于水质消毒 | D. | 氧化铁常用作红色油漆和涂料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com