
| 10-14 |
| 10-5 |


科目:高中化学 来源: 题型:
| A、室温下,向0.01 mol?L-1的NH4HSO4溶液中滴加NaOH溶液至中性:C(Na+)>C(SO42-)>C(NH4+)>C(OH-)=C(H+) |
| B、0.1 mol?L-1的NaHCO3溶液:C(Na+)>C(OH-)>C(HCO3-)>C(H+) |
| C、Na2CO3溶液:C(OH-)-C(H+)=C(HCO3-)+C(H2CO3) |
| D、25℃时,浓度均为0.1 mol?L-1的CH3COOH、CH3COONa混合溶液,呈酸性:C(CH3COO-)+C(OH-)<C(CH3COOH)+C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
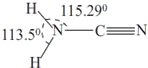
| A、既有酸性也有碱性 |
| B、既能溶于水,又能溶于乙醇 |
| C、分子内σ键与π键数目之比为1:1 |
| D、分子内中所有原子共面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
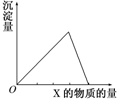 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为NaAlO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2和氯气都能使品红褪色 | 两者都有漂白性 |
| B | Al(OH)3是两性氢氧化物 | 盐酸和氨水能溶解Al(OH)3 |
| C | 镁能与氮气发生反应 | 镁是活泼金属,有较强的还原性 |
| D | 氯化氢气体不导电,盐酸导电 | 两者都属于电解质 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水电离出来的c(OH-)=1.0×10-13mol?L-1 |
| B、该溶液的pH<13 |
| C、溶液中离子浓度关系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、加入等浓度等体积的盐酸,溶液中:c(CH3COOH)+c(CH3COO-)=c(Cl-)+c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
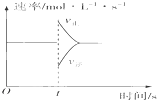 在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用右图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )
在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用右图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )| A、对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和体积不变,再加入一定量的HI |
| B、对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和压强不变,再加入一定量的HI |
| C、对于PCl5(g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和体积不变,再加入一定量的PCl5 |
| D、对于PCl5 (g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和压强不变,再加入一定量的PCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com