
 ;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
;写出蓝色沉淀溶解在氨水中的离子方程式Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O. 分析 [Cu(NH3)4]2+为深蓝色离子,向CuSO4溶液中逐滴加入氨水至过量,先生成氢氧化铜,再加过量的氨水氨水与氢氧化铜生成铜氨络离子,[Cu(NH3)4]2+为配合物,Cu2+为中心离子,电荷数为+2,NH3为配体,配位数为4.
解答 解:向CuSO4的水溶液中逐滴加入氨水,离子方程式为:Cu2++2NH3•H2O=Cu(OH)2↓+2H2O,至过量,观察到溶液由天蓝色最终变为深蓝色,生成[Cu(NH3)4]2+,反应的离子方程式为:Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O,[Cu(NH3)4]2+的结构式为 ,
,
故答案为: ;Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
;Cu(OH)2+4NH3•H2O=[Cu(NH3)4]2++2OH-+4H2O.
点评 本题考查了配合物的组成及性质,题目难度不大,注意配合物深蓝色的离子的结构式中的成键.


科目:高中化学 来源: 题型:选择题
| 选项 | 环境要求 | 离子组 |
| A | Fe2(SO4)3溶液中 | K+、AlO2-、Cl-、NO3- |
| B | 与Al反应能放出H2的溶液中 | Fe2+、Na+、NO3-、SO42- |
| C | 水电离产生的c(H+)=10-12mol/L的溶液 | ClO-、CO32-、NH4+、NO3-、SO32- |
| D | 向溶液中逐滴滴加烧碱溶液先有沉淀产生,后沉淀消失 | Na+、Al3+、Cl-、SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
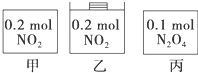 甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )| A. | 平衡时各容器内n(NO2)的大小顺序为乙>甲>丙 | |
| B. | 平衡时NO2的百分含量:乙>甲=丙 | |
| C. | 平衡时甲中NO2与丙中N2O4的转化率一定相同 | |
| D. | 平衡时混合物的平均相对分子质量:乙>甲=丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
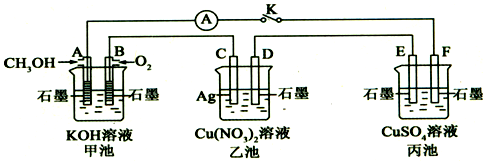
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):
A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol(反应热) | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食醋可用于除去暖水瓶中的水垢 | B. | 纯碱可除去灶具上的油污 | ||
| C. | 酒精可用于杀菌消毒 | D. | 单质硅可用作光缆 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com