
 Ģ«ŃōÄܵē³Ų³£ÓĆ²ÄĮĻ³żµ„¾§¹č£¬»¹ÓŠĶī÷ļŲĪųµČ»ÆŗĻĪļ£®
Ģ«ŃōÄܵē³Ų³£ÓĆ²ÄĮĻ³żµ„¾§¹č£¬»¹ÓŠĶī÷ļŲĪųµČ»ÆŗĻĪļ£®·ÖĪö £Ø1£©ļŲŹĒ31ŗÅŌŖĖŲ£¬øł¾ŻŌ×ÓŗĖĶāµē×ÓÅŲ¼¹ęĀÉæÉŅŌŠ“³öµē×ÓÅŲ¼Ź½£»
£Ø2£©É锢Īų”¢äåČżÖÖŌŖĖŲ¶¼ŹĒµŚ4ÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«ÉéŌŖĖŲŌ×Ó4pÄܼ¶ŹĒ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚĶ¬ÖÜĘŚĻąĮŚŌŖĖŲ£¬¹ŹµŚŅ»µēĄėÄÜBr£¾As£¾Se£¬¾Ż“Ė“šĢā£»
£Ø3£©ĘųĢ¬SeO3·Ö×ÓÖŠÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹżæÉŅŌÅŠ¶Ļ·Ö×Ó¹¹ŠĶ£»
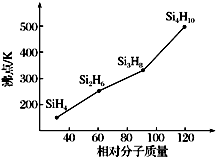
£Ø4£©¹čĶé£ØSinH2n+2£©¶¼ŹĒ·Ö×Ó¾§Ģ壬·Ö×Ó¾§ĢåµÄ·ŠµćøßµĶČ”¾öÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¶ų·Ö×Ó¼ä×÷ÓĆĮ¦ÓėĻą¶Ō·Ö×ÓÖŹĮæµÄ“óŠ”ÓŠ¹Ų£¬¾Ż“Ė“šĢā£»
£Ø5£©øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪČ·¶ØĘäŌӻƷ½Ź½£»
£Ø6£©øł¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŠŌŖĖŲŗĶµēŗÉŹŲŗć£¬æÉŠ“³öĄė×Ó·½³ĢŹ½£»
£Ø7£©ĄūÓĆ¾łĢƷؼĘĖćĮ½ÖÖ½šŹōŌ×ÓøöŹżÖ®±Č£¬øł¾Ż¦Ń=$\frac{m}{V}$¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©ļŲŹĒ31ŗÅŌŖĖŲ£¬øł¾ŻŌ×ÓŗĖĶāµē×ÓÅŲ¼¹ęĀÉæÉŅŌŠ“³öµē×ÓÅŲ¼Ź½ĪŖ£ŗ1s22s22p63s23p63d104s24p1£Ø»ņ[Ar]3d104s24p1£©£¬
¹Ź“š°øĪŖ£ŗ1s22s22p63s23p63d104s24p1£Ø»ņ[Ar]3d104s24p1£©£»
£Ø2£©É锢Īų”¢äåČżÖÖŌŖĖŲ¶¼ŹĒµŚ4ÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµŚŅ»µēĄėÄܳŹŌö“óĒ÷ŹĘ£¬µ«ÉéŌŖĖŲŌ×Ó4pÄܼ¶ŹĒ°ėĀśĪȶØדĢ¬£¬ÄÜĮæ½ĻµĶ£¬µŚŅ»µēĄėÄÜøßÓŚĶ¬ÖÜĘŚĻąĮŚŌŖĖŲ£¬¹ŹµŚŅ»µēĄėÄÜBr£¾As£¾Se£¬¹Ź“š°øĪŖ£ŗBr£¾As£¾Se£»
£Ø3£©ĘųĢ¬SeO3·Ö×ÓÖŠÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹżĪŖ$\frac{6+0}{2}$=3£¬ĪŽ¹Āµē×Ó¶Ō£¬ĖłŅŌ·Ö×Ó¹¹ŠĶĪŖĘ½ĆęČż½ĒŠĪ£¬
¹Ź“š°øĪŖ£ŗĘ½ĆęČż½ĒŠĪ£»
£Ø4£©¹čĶé£ØSinH2n+2£©¶¼ŹĒ·Ö×Ó¾§Ģ壬·Ö×Ó¾§ĢåµÄ·ŠµćøßµĶČ”¾öÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¶ų·Ö×Ó¼ä×÷ÓĆĮ¦ÓėĻą¶Ō·Ö×ÓÖŹĮæµÄ“óŠ”ÓŠ¹Ų£¬¹čĶéµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“󣬷Ö×Ӽ䷶µĀ»ŖĮ¦Ō½Ē棬
¹Ź“š°øĪŖ£ŗ¹čĶéµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“󣬷Ö×Ӽ䷶µĀ»ŖĮ¦Ō½Ē棻
£Ø5£©[B£ØOH£©4]-ÖŠBµÄ¼Ū²ćµē×Ó¶Ō=4+$\frac{1}{2}$£Ø3+1-4”Į1£©=4£¬ĖłŅŌ²ÉČ”sp3Ōӻƣ¬¹Ź“š°øĪŖ£ŗsp3£»
£Ø6£©½šŹōCuµ„¶ĄÓė°±Ė®»ņµ„¶ĄÓė¹żŃõ»ÆĒā¶¼²»ÄÜ·“Ó¦£¬µ«æÉÓė°±Ė®ŗĶ¹żŃõ»ÆĒāµÄ»ģŗĻČÜŅŗ·“Ó¦£¬ĖµĆ÷Į½ÕßÄÜ»„Ļą“Ł½ų£¬ŹĒĮ½ÖÖĪļÖŹ¹²Ķ¬×÷ÓĆµÄ½į¹ū£¬ĘäÖŠ¹żŃõ»ÆĒāĪŖŃõ»Æ¼Į£¬°±ÓėCu2+ŠĪ³ÉÅäĄė×Ó£¬Į½ÕßĻą»„“Ł½ųŹ¹·“Ó¦½ųŠŠ£¬·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCu+H2O2+4NH3•H2O=Cu£ØNH3£©42++2OH-+4H2O£¬
¹Ź“š°øĪŖ£ŗCu+H2O2+4NH3•H2O=Cu£ØNH3£©42++2OH-+4H2O£»
£Ø7£©ŌŚ¾§°ūÖŠ£¬AuŌ×ÓĪ»ÓŚ¶„µć£¬CuŌ×ÓĪ»ÓŚĆęŠÄ£¬øĆ¾§°ūÖŠAuŌ×ÓøöŹż=8”Į$\frac{1}{8}$=1£¬CuŌ×ÓøöŹż=6”Į$\frac{1}{2}$=3£¬ĖłŅŌøĆŗĻ½šÖŠAuŌ×ÓÓėCuŌ×ÓøöŹżÖ®±Č=1£ŗ3£¬
¾§°ūĢå»żV=£Øa”Į10-10cm£©3£¬Ćæøö¾§°ūÖŠĶŌ×ÓøöŹżŹĒ3”¢AuŌ×ÓøöŹżŹĒ1£¬Ōņ¦Ń=$\frac{\frac{197+64”Į3}{{N}_{A}}}{£Øa”Į1{0}^{-10}£©^{3}}$£¬
¹Ź“š°øĪŖ£ŗ1£ŗ3£»$\frac{\frac{197+64”Į3}{{N}_{A}}}{£Øa”Į1{0}^{-10}£©^{3}}$£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖŗĖĶāµē×ÓÅŲ¼”¢µŚŅ»µēĄėÄÜ”¢·Ö×Óæռ乹ŠĶ”¢ŌӻƷ½Ź½”¢¾§°ūĆÜ¶ČµÄ¼ĘĖć£¬ÄѶČÖŠµČ£¬½āĢāŹ±ŅŖ×¢Ņā¶Ō»ł±¾ÖŖŹ¶µÄĮé»īŌĖÓĆ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
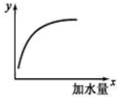 ČēĶ¼±ķŹ¾ 25”ꏱ£¬Ļņ 1L£¬0.1mol•L-1µÄŅ»ŌŖČõĖįHAÖŠ¼ÓĖ®Ļ”ŹĶ¹ż³ĢµÄ±ä»ÆĶ¼Ļó£¬ŌņĶ¼ÖŠ×Ż×ų±źy±ķŹ¾µÄŹĒ£Ø””””£©
ČēĶ¼±ķŹ¾ 25”ꏱ£¬Ļņ 1L£¬0.1mol•L-1µÄŅ»ŌŖČõĖįHAÖŠ¼ÓĖ®Ļ”ŹĶ¹ż³ĢµÄ±ä»ÆĶ¼Ļó£¬ŌņĶ¼ÖŠ×Ż×ų±źy±ķŹ¾µÄŹĒ£Ø””””£©| A£® | c£ØH+£©»ņ c£ØOH-£© | B£® | HAµÄµēĄėĘ½ŗā³£ŹżKa | ||
| C£® | c£ØH+£©/c£ØHA£© | D£® | n£ØH+£©»ņ n£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.4mol•L-1 | B£® | 1.2mol•L-1 | C£® | 1.1mol•L-1 | D£® | 1.0mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ź³ŃĪĖ® | B£® | Ź³“× | C£® | ŹÆ»ŅĖ® | D£® | “æ¾»Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬11.2L±½ÖŠŗ¬ÓŠ·Ö×ӵďżÄæĪŖ0.5NA | |
| B£® | 0.1mol±ūĻ©ĖįÖŠŗ¬ÓŠĖ«¼üµÄŹżÄæĪŖ0.1NA | |
| C£® | 1.6gÓÉŃõĘųŗĶ³ōŃõ×é³ÉµÄ»ģŗĻĪļÖŠŗ¬ÓŠŃõŌ×ӵďżÄæĪŖ0.1NA | |
| D£® | ŌŚ¹żŃõ»ÆÄĘÓėĖ®µÄ·“Ó¦ÖŠ£¬ĆæÉś³É0.1molŃõĘų£¬×ŖŅʵē×ӵďżÄæĪŖ0.4NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X”¢YĮ½ÖÖŌŖĖŲæÉÄÜÄÜŠĪ³É¶ąÖÖ»ÆŗĻĪļ | |
| B£® | X”¢YÖŠXµÄĒā»ÆĪļµÄĪČ¶ØŠŌĒæ | |
| C£® | Ńõ»ÆĪļÄÜŗĶĒāŃõ»ÆÄĘ·“Ó¦µÄŌŖĖŲæÉÄÜÓŠ4ÖÖ | |
| D£® | ŌŖĖŲWµÄijŠ©»ÆŗĻĪļæÉ×÷ĪŖĖ®“¦Ąķ¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆĢśÓėĒāµāĖį·“Ó¦£ŗFe£ØOH£©3+3H+ØTFe3++3H2O | |
| B£® | Ļņ·ŠĖ®ÖŠµĪ¼Ó±„ŗĶµÄĀČ»ÆĢśČÜŅŗ£ŗFe3++3H2OØTFe£ØOH£©3”ż+3H+ | |
| C£® | FeBr2ČÜŅŗÖŠĶØČė×ćĮæCl2£ŗ2Fe2++2Br-+2Cl2=2Fe3++Br2++4Cl- | |
| D£® | ĻņFeCl2ČÜŅŗÖŠ¼ÓČėÉŁĮæK3[Fe£ØCN£©6]ČÜŅŗ£ŗ3Fe2++2[Fe£ØCN£©6]3-ØTFe3[Fe£ØCN£©6]2”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Y·Ö±šÓėZ”¢WŠĪ³ÉµÄ»ÆŗĻĪļÖŠ»Æѧ¼üĄąŠĶĻąĶ¬ | |
| B£® | Ō×Ó°ė¾¶µÄ“óŠ”Ė³Šņ£ŗr£ØW£©£¾r£ØZ£©£¾r£ØY£©£¾r£ØX£© | |
| C£® | YµÄĘųĢ¬¼ņµ„Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČWµÄĒæ | |
| D£® | XµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌ±ČWµÄČõ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com