
| A、X、Y的简单离子半径:r(X2-)<r(Y+) |
| B、M的气态氢化物比N的气态氢化物稳定 |
| C、M与X形成的化合物对应的水化物一定是强酸 |
| D、Y2X和Y2X2中阴、阳离子的个数比相同,但化学键类型不同 |


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
| A、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| B、减少资源消耗,增加资源的重复利用、资源的循环再生 |
| C、发展低碳经济,推广利用电能、风能的城市照明系统 |
| D、大力开采煤、石油和天然气以满足人们日益增长的能源需求 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3+H2O=H2SO4 |
| B、2Na2O2+2H2O=4NaOH+O2↑ |
| C、2F2+2H2O=4HF+O2 |
| D、NaH+H2O=NaOH+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定管装滴定液时应先用滴定液润洗 |
| B、锥形瓶用作反应容器时一定不能加热 |
| C、蒸馏时温度计水银球可以高于蒸馏瓶支管口 |
| D、萃取时振荡分液漏斗应关闭其玻璃塞并打开活塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油裂解得到的汽油是纯净物 |
| B、石油产品都可用于聚合反应 |
| C、水煤气是通过煤的液化得到的气体燃料 |
| D、石油主要含有碳、氢两种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体一定是混合物 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体属于介稳体系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、1:3 | B、3:1 |
| C、1:2 | D、2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、.先有S生成 |
| B、.先有I2生成 |
| C、.先有Br2生成 |
| D、.以上结论均不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
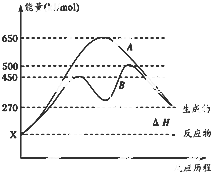 (1)已知:①Fe(s)+
(1)已知:①Fe(s)+| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com