
下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤电镀过程相当于金属的“迁移”,可视为物理变化
A.①②③④  B
B .③④
.③④
C.③④⑤ D.④
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
对于反应CO(g)+H2O(g)  CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下( )
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下( )
A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变
B.改变压强,平衡不发生移动,反应放出的热量不变
C.升高温度,反应速率加快,反应放出的热量不变
D.若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
经测定,H2O2为二元弱酸,其酸性比碳酸弱,它在碱性溶液中极不稳定,易分解生成H2O和O2。若向Na2O2中通入干燥的CO2气体,Na2O2与CO2并不起反应。
(1)写出H2O2在水溶液中的电离方程式
(2)用化学方程式表示Na2O2和潮湿的CO2气体反应的过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
丙二酸(H2A)的pKa1 = 2.86,pKa2 = 5.70,向20.00 mL Na2A、NaHA混合溶液中加入1.00 mL 0.0100 mol·L-1 HCl,pH为5.70;滴入同样浓度10.00 mL HCI,pH为4.28,求初始混合液中Na2A、NaHA浓度和pH。
查看答案和解析>>
科目:高中化学 来源: 题型:
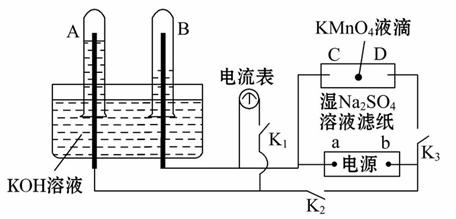
在如图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹夹在被Na2SO4溶液浸湿的滤纸条上。滤纸条的中部滴有KMnO4液滴;电源有a、b两极。在A、B 中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3,通直流电。
(1)写出B中电极反应式____________________________________________ ___。
___。
(2)在湿的硫酸钠溶液滤纸条中部的高锰酸钾液滴处发生的现象是__________。
(3)电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针__________(填“是”或“否”)移动,其理由是_____________。
(4)在298 K时,若2 g B气体和0.5 mol的A气体完全反应,生成物为液态,放出285.8 kJ热量,写出此反应的热化学方程式:______________________
__________ ________________________________________________________。
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在碱性溶液中能大量共存且为无色透明的溶液是( )
|
| A. | K+、Cl﹣、MnO4﹣、SO42﹣ | B. | Na+、Cu2+、NO3﹣、CO32﹣ |
|
| C. | Na+、NO3﹣、SO42﹣、HCO3﹣ | D. | Na+、SO42﹣、Cl﹣、NO3﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
请回答下列问题:
(1)T的原子结构示意图为 .
(2)元素的非金属性为(原子的得电子能力):Q W(填“强于”或“弱于”).
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 .
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 .
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 .
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ.又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H= (注:题中所涉单质均为最稳定单质).

查看答案和解析>>
科目:高中化学 来源: 题型:
某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等.水垢会形成安全隐患,需及时清洗除去.清洗流程如下:
Ⅰ.加入NaOH 和 Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉.
(资料在线:K3[Fe(CN)6]溶液遇亚铁盐会生成蓝色沉淀.)
(1)用NaOH溶解二氧化硅的化学方程式是 .
(2)在步骤Ⅱ中:
①被除掉的水垢除铁锈外,还有 .
②清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因 .
(3)步骤Ⅲ中,加入Na2SO3的目的是 .
(4)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe3O4保护膜.
①完成并配平其反应的离子方程式:
Fe+ NO2+ H2O═ N2↑+ +
②钝化效果的检测一般可用滤纸浸渍配好的检测液后贴附于待测样品表面或直接将溶液涂、滴于待测表面.下面检测钝化效果的方法合理的是 .
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
d.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com