
| A. | 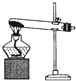 加热分解NaHCO3 | B. | 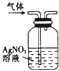 除去氯气中的少量氯化氢 | ||
| C. | 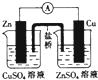 构成铜锌原电池 | D. | 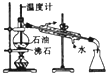 分馏石油 |
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH | |
| B. | 用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 | |
| C. | 在铁件上镀铜时,金属铜作阴极 | |
| D. | 电解精炼铜时,电解质溶液中铜离子浓度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Cu2+ K+ Na+ SO42- | B. | K+ Na+ Cl-HCO3- | ||
| C. | Cl- NO3- Mg2+ NH4+ | D. | NO3- Na+ Cl-K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、NO3-、SiO32- | B. | H+、NH4+、Al3+、SO42- | ||
| C. | Fe2+、H+、ClO-、SO42- | D. | AlO2-、Mg2+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.
.该元素的原子序数为21,该元素是金属元素(填“金属”或“非金属”),形成的单质为金属晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实 验 事 实 | 结 论 |
| A | BaSO4难溶于水,NH3的水溶液导电 | BaSO4是非电解质,NH3是电解质 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | 等体积,H+浓度相同的盐酸和醋酸同时分别与少量等质量的形状相同的锌粒反应 | 产生氢气的质量相同 |
| D | 在容积可变的密闭容器中发生反应: H2(g)+I2(g)?2HI(g),把容积缩小一倍 | 正反应速率加快,逆反应速率不变 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com