
下列有关实验操作和说法正确的是( )
|
| A. | 用pH试纸检验气体的酸碱性时,一定要先用蒸馏水润湿 |
|
| B. | 润洗滴定管:从滴定管上口加入所要盛装的酸或碱溶液至“0”刻线,再将液体从滴定管下部放出,重复操作2~3次 |
|
| C. | 用瓷坩埚加热熔化碳酸钠固体 |
|
| D. | Mg和Al分别为电极,插入NaOH溶液中,构成原电池,探究Mg、Al的活泼性 |
| 测定溶液pH的方法;原电池和电解池的工作原理;过滤、分离与注入溶液的仪器. | |
| 分析: | A、用pH试纸可以测出酸碱性,但不能测pH值【气体也就无所谓pH】; B、润洗滴定管应用水洗、待装液洗,加入少量,不能加入到0刻度; C、碳酸钠熔融和二氧化硅反应; D、镁铝在氢氧化钠溶液中形成原电池反应,铝做负极. |
| 解答: | 解:A、用pH试纸可以测出酸碱性,但不能测pH值,气体只能溶于水显示酸碱性,故A正确; B、润洗滴定管应用水洗、待装液洗,加入少量,不能加入到0刻度,浪费试剂,故B错误; C、瓷坩埚主要成分含有二氧化硅,碳酸钠熔融和二氧化硅反应,不能用来加热碳酸钠,故C错误; D、镁铝在氢氧化钠溶液中形成原电池反应,铝做负极,但铝活泼性小于镁,不能作为金属性的比较方法,故D错误; 故选A. |
| 点评: | 本题考查了溶液酸碱性分析测定,原电池原理,实验基本操作,掌握基础是关键,题目较简单. |


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
为了探究“氯气的性质和用途”,某学习小组以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行实验.
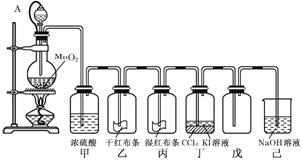
试回答下列问题:
(1)乙中的现象是____________________,丙中的现象是______________,丁中的现象是______________,分离丁中液体的方法是____________;
(2)橡皮管连通后,分液漏斗中的气体压强p1与烧瓶中的气体压强p2的关系为________(填“>”“<”或“=”),连接橡皮管的目的是_______________________;
(3)烧瓶内发生反应的离子方程式为_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 L HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6 mol/l,向该溶液中加入足量铜粉,加热,充分反应,当HNO3与H2SO4的物质的量比为x:y 时所得溶液中Cu2+物质的量浓度最大,则x:y为
A.2:3 B.3:8 C.1:4 D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知木炭在一定条件下与浓硝酸反应生成两种+4价的氧化物,为了探究一氧化氮(NO)能否与过氧化钠反应,以及反应后的产物中是否有亚硝酸钠(NaNO2), 某小组同学设计了如图所示装置(夹持仪器和连接用的乳胶管已经省略)。
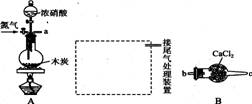

(1)为了完成该实验,虚线框内还需要连接B~E四套装置,按气流方向连接的顺序为a→( )( ) →( )( ) →( )( ) →( )( )(填仪器接口的字母编号)。连接好仪器,检查气密性,装入药品后,要通入一段时间的氮气,再滴加浓硝酸,点燃酒精灯,通人氮气的主要目的是 。
(2)简述使用分液漏斗向圆底烧瓶中滴加浓硝酸的操作: 。装置E中观察到的主要实验现象有 。
(3)装置C的作用是 。
(4)某同学经查阅资料后发现亚硝酸是弱酸,性质不稳定,室温下易分解成一氧化氮。装置D中充分反应后,设计实验证明D中是否有亚硝酸钠生成: (写出检验步骤及现象)。
(5)亚硝酸钠在酸性条件下可将I一氧化为I2,该反应常用于亚硝酸钠含量的测定,请写出该反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知同温同压下,下列反应的焓变和平衡常数分别表示为
H2(g)+ O2(g)=H2O(g)△H1 K1
O2(g)=H2O(g)△H1 K1
 N2(g)+O2(g)=NO2(g)△H2 K2
N2(g)+O2(g)=NO2(g)△H2 K2
 N2(g)+
N2(g)+ H2(g)=NH3(g)△H3 K3
H2(g)=NH3(g)△H3 K3
则反应2NH3(g)+ O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
O2(g)=2NO2(g)+3H2O(g)的△H和K分别为( )
|
| A. | 2△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
|
| B. | 2△H3﹣3△H1﹣2△H2 |
|
| C. | 3△H1+2△H2﹣2△H3 |
|
| D. | 3△H1+2△H2﹣2△H3 3K1+2K2﹣2K3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将Na2CO3和NaHCO3混合物〔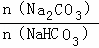 =a a≤3〕溶于水制得稀溶液,下列有关该溶液中微粒的物质的量浓度关系正确的是( )
=a a≤3〕溶于水制得稀溶液,下列有关该溶液中微粒的物质的量浓度关系正确的是( )
|
| A. | a=1则c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+) |
|
| B. | a=2则c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3) |
|
| C. | a为任意值时,则c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣) |
|
| D. | a=0则c(Na+)>c(HCO3﹣)>c(CO32﹣)>c(OH﹣)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度T℃下,某Ba(OH)2稀溶液中c(H+)=10﹣amol/L,c(OH﹣)=10﹣bmol/L,已知a+b=12,向该溶液中逐滴加入NaHSO4溶液,测得混合溶液的部分PH如下表所示:
| 序号 | 氢氧化钡的体积/mL | 硫酸氢钠的体积/mL | 溶液的PH |
| ① | 33.00 | 0.00 | 8 |
| ② | 33.00 | X | 7 |
| ③ | 33.00 | 33.00 | 6 |
(1)依据题意判断,T℃ 大于 25℃(填“大于”、“小于”或“等于”)
(2)b= 4 ,X= 27
(3)反应③的离子方程式为: Ba2++2OH﹣+2H++SO42﹣=BaSO4↓+2H2O
(4)将此温度下的Ba(OH)2溶液取出1mL,加水稀释至1L,则稀释后溶液中c(Ba2+):c(OH﹣) 1:20 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定密闭容器中,反应aA(g)═bB(g)达平衡后,保持温度及各物质的量不变,将容器体积增加1倍,当达到新平衡时,B的浓度是原来的60%,则下列说法不正确的是( )
|
| A. | 平衡向正反应方向移动了 |
|
| B. | 物质A的转化率减少了 |
|
| C. | 容器体积增加可以是向其中充入了惰性气体 |
|
| D. | a<b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com