
 运用碳及其化合物的性质,完成下列小题:
运用碳及其化合物的性质,完成下列小题:分析 (1)根据石灰水能与空气中的二氧化碳反应生成碳酸钙白色沉淀;碳酸钙难溶于水,能与酸反应,可用稀盐酸洗去;进行分析解答;
(2)碳酸氢钠加热分解生成碳酸钠,而碳酸钠比较稳定,可以用加热的方法除去碳酸钠固体中碳酸氢钠;
(3)向碳酸氢钠溶液滴加NaOH溶液,发生反应的离子方程式为OH-+HCO3-=H2O+CO32-.
解答 解:(1)石灰水中的溶质是氢氧化钙,能与空气中的二氧化碳反应生成碳酸钙沉淀和水;由于碳酸钙是一种不溶于水的白色物质,故瓶中常形成一种不溶于水的白色固体;反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O;
碳酸钙难溶于水,能与酸反应,实验室洗涤该试剂瓶可用稀盐酸洗去,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
故答案为:CO2+Ca(OH)2=CaCO3↓+H2O;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)碳酸钠比较稳定,而碳酸氢钠加热分解生成碳酸钠、二氧化碳和水,故可用加热的方法来除去碳酸氢钠,反应方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3 +CO2↑+H2O,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3 +CO2↑+H2O;
(3)向碳酸氢钠溶液滴加NaOH溶液,发生反应的离子方程式为OH-+HCO3-=H2O+CO32-,故答案为:OH-+HCO3-=H2O+CO32-.
点评 本题考查化学方程式和离子方程式的书写,难度不大,掌握二氧化碳的化学性质并能灵活运用是正确解答本题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 在蒸馏水中滴加浓H2SO4,Kw不变 | |
| B. | CaCO3不易溶于稀硫酸,也不易溶于醋酸 | |
| C. | NaCI溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| D. | 在Na2S稀溶液中,c(H+)=c( OH-)-2c(H2S)-c(HS-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5υ(O2)=4υ(NH3) | B. | 6υ(H2O)=5υ(O2) | C. | 3υ(H2O)=2υ(NH3) | D. | 5υ(NO)=4υ(O2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1的某二元弱碱的酸式盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| B. | 25℃时,pH=12的氨水和pH=12的盐酸等体积混合:c(Cl-)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| C. | 等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合:c(OH-)=c(H+)+c(CH3COOH) | |
| D. | 向NH4HSO4溶液中加入等物质的量的NaOH形成的溶液中:c(Na+)=c(SO${\;}_{4}^{2-}$)+c(NH${\;}_{4}^{+}$)+c(H+)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
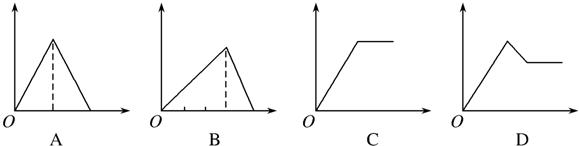
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 事实或实验 | 结论 |
| A | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| B | 向某溶液中滴加氯水,再加入KSCN溶液,溶液呈红色 | 原溶液中一定含有Fe2+ |
| C | 汽车尾气净化反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△S<0 | 该反应在常温不能自发进行 |
| D | 向NaBr溶液中滴入少量氯水和CCl4,振荡,静置溶液下层呈红色 | Br-还原性强于Cl- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
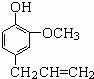 丁子香酚存在于丁香油、樟脑油等中,常用于配制康乃馨型香精以及制异丁香酚和香兰素等,也用作杀虫剂和防腐剂.丁子香酚结构简式如图:
丁子香酚存在于丁香油、樟脑油等中,常用于配制康乃馨型香精以及制异丁香酚和香兰素等,也用作杀虫剂和防腐剂.丁子香酚结构简式如图: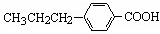 、
、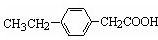 .
.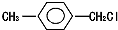 和乙醇为原料制备丁子香酚的一种同分异构体:对-甲基苯甲酸乙酯的合成路线(无机试剂任选).
和乙醇为原料制备丁子香酚的一种同分异构体:对-甲基苯甲酸乙酯的合成路线(无机试剂任选).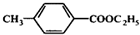
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com