

分析 Ⅰ.装置A中铁与氯气反应,反应为:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品;为防止外界空气中的水蒸气进入装置使FeCl3潮解,所以用装置C无水氯化钙来吸水,装置D中用FeCl2吸收Cl2时的反应离子方程式2Fe2++Cl2═2Fe3++2Cl-,用装置D中的副产品FeCl3溶液吸收H2S,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,所以装置E为氢氧化钠溶液吸收氯气.
(1)装置A中铁与氯气反应生成氯化铁;
(2)要使沉积的FeCl3进入收集器,根据FeCl3加热易升华的性质;
(3)防止FeCl3潮解,不与水蒸气接触;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品;装置C的名称为干燥管;检验FeCl2是否失效应检验FeCl2是否存在,可以用KMnO4溶液检验;用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸;
Ⅱ.(5)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应;
(6)电解氯化亚铁时,阴极阳离子得到电子发生还原反应;阳极阳离子失去电子发生氧化反应.
解答 解:Ⅰ.(1)氯气具有强氧化性,将变价铁氧化成高价铁,生成氯化铁,所以装置A中铁与氯气反应生成氯化铁,反应为2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,
故答案为:2Fe+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3;
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,第④步操作是对FeCl3加热发生升华使沉积的FeCl3进入收集器,
故答案为:在沉积的FeCl3固体下方加热;
(3)为防止FeCl3潮解所采取的措施有②通入干燥的Cl2⑤用干燥的N2赶尽Cl2,故选:②⑤;
(4)B中的冷水作用为是冷却FeCl3使其沉积,便于收集产品,装置C的名称为干燥管;
检验FeCl2是否失效,应检验FeCl2是否存在,可以用KMnO4溶液检验;
用氢氧化钠溶液吸收的是氯气,不用考虑防倒吸,
故答案为:冷却,使FeCl3沉积,便于收集产品;干燥管;KMnO4溶液; ;
;
Ⅱ.(5)三价铁具有氧化性,硫化氢具有还原性,二者之间发生氧化还原反应:2FeCl3+3H2S=2FeCl2+6HCl+3S↓,离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,
故答案为:2Fe3++H2S=2Fe2++S↓+2H+;
(6)电解氯化亚铁时,阴极发生氢离子得电子的还原反应,2H++2e-═H 2↑,阳极亚铁离子发生失电子的氧化反应:Fe2+-e-=Fe3+,
故答案为:Fe2+-e-=Fe3+.
点评 本题考查了制备无水FeCl3实验操作和实验设计,题目难度中等,侧重考查铁、氯、硫及其化合物的性质应用、实验基本操作的分析判断、实验现象的推断和应用,试题综合性较强,有利于培养学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 检验步骤 | 实验操作 | 实验现象 | 结论 | |
| 步骤一 | 取少量反应后的溶液,加入稀盐酸 | 有气泡产生 | ||
| 步骤二 | 将步骤一产生的气体通入澄清石灰水 | 澄清石灰水变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 序号 | 操作 | 可能出现的现象 | 结论 |
| ① | 向a试管中滴加几滴0.01mol/L的KMnO4(或溴水)溶液 | 若溶液褪色 | 则假设1成立 |
| 若溶液不褪色 | 则假设2或3成立 | ||
| ② | 向b试管中滴加几滴品红溶液 | 若溶液褪色 | 则假设1或3成立 |
| 若溶液不褪色 | 假设2成立 | ||
| ③ | 向C试管中滴加几滴淀粉-KI溶液 | 若溶液变为蓝色 | 假设3成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知可逆反应:2SO2+O2?2SO3,当O2的消耗速率与SO3的消耗速率之比为1:2时,表明该可逆反应达到化学平衡状态 | |
| B. | 由Zn、Cu、稀硫酸组成的原电池,负极为Zn,发生还原反应,电极反应式为:Zn-2e-=Zn2+ | |
| C. | 工业上金属Mg、Al都是用电解熔融的氯化物制得的 | |
| D. | 甲苯的一氯代物有4种,则甲苯与足量H2发生加成反应后所得到的有机产物的一氯代物也只有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


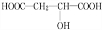 +HCOOH$?_{△}^{浓硫酸}$
+HCOOH$?_{△}^{浓硫酸}$ +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com