
(12分)(1)氮元素基态原子核外未成对电子数为 个;
(2)C、N、O三种元素第一电离能从大到小的顺序是_____________;
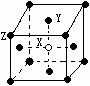
(3)某晶体的晶胞如图所示,X位于体心,Y位于4个面心,Z位于8个顶点,该晶体中 X、Y、Z的粒子个数比为______________;
(4)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态
电子排布式 ;葡萄糖分子中碳原子杂化方式有 。
(5)某化合物其组成可用CoCl3·5NH3表示。把CoCl3·5NH3溶于水后立即加硝酸银溶液,则析出AgCl沉淀。经测定,每1 mol CoCl3·5NH3只生成2 mol AgCl。请写出表示此配合物结构的化学式(钴的配位数为6)_____________________。
(12分,每空2分)(1)3 (2分)
(2)N、O 、C (2分) (3)1∶2∶1 (2分)
(4)1s22s22p63s23p63d10 或[Ar] 3d10 (2分) sp2、sp3(2分)
(5)[Co(NH3)5Cl]Cl2 (2分)
【解析】(1)根据构造原理可知,氮元素基态原子核外电子排布式为11s22s22p3,所以未成对电子数为3个。
(2)非金属性越强,第一电离能越大,但由于氮原子的2p轨道是半充满状态,稳定性强,所以氮元素的第一电离能大于氧元素的,即顺序是N>O>C 。
(3)X位于体心,Y位于4个面心,Z位于8个顶点,所以该晶胞中含有的X、Y、Z原子数分别是1、4×1/2=2、8×1/8=1,因此晶体中 X、Y、Z的粒子个数比为1∶2∶1 。
(4)根据构造原理可知Zn2+基态电子排布式为1s22s22p63s23p63d10 或[Ar] 3d10。分子中5个饱和碳原子全部形成单键,所以是sp3杂化。而羧基中的碳原子含有碳养双键,所以是sp2杂化。
(5)1 mol CoCl3·5NH3只生成2 mol AgCl,说明作为配体的氯离子只有1个,所以配合物结构的化学式[Co(NH3)5Cl]Cl2 。


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| H | + 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ).
).查看答案和解析>>
科目:高中化学 来源:2010年福建省华安一中高二下学期期末考试化学试题 题型:填空题
(9分)氮及其化合物在生活、生产和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为 ;
(2)在氮气分子中,氮原子之间存放着 个σ键和 个π键;
(3)N2分子中氮氮键的键长 (填“大于”、“小于”或“等于”)
F2分子中氟氟键的键长;
(4)氮元素的氢化物——NH3是一种易液化的气体,该气体易液化的原因
是 。
(5)配合物[Cu(NH3)4]C12中含有4个配位键,若用2个N2H4代替其中2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]C12中含有配位键的个数为 。
查看答案和解析>>
科目:高中化学 来源:2010年福建省高二下学期期末考试化学试题 题型:填空题
(9分)氮及其化合物在生活、生产和科技等方面有重要的应用。请回答下列问题:
(1)氮元素基态原子的价电子排布式为 ;
(2)在氮气分子中,氮原子之间存放着 个σ键和 个π键;
(3)N2分子中氮氮键的键长 (填“大于”、“小于”或“等于”)
F2分子中氟氟键的键长;
(4)氮元素的氢化物——NH3是一种易液化的气体,该气体易液化的原因
是 。
(5)配合物[Cu(NH3)4]C12中含有4个配位键,若用2个N2H4代替其中2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]C12中含有配位键的个数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com