
| A. | 乙烷(乙炔):将混合气体通过酸性高锰酸钾溶液,洗气除去乙烷中的乙炔气体 | |
| B. | 苯(苯酚):向混合液中加入适量的浓溴水,过滤,除去苯中的少量苯酚 | |
| C. | 酒精(水):向含水酒精中加入生石灰,蒸馏,得到无水酒精 | |
| D. | 硝基苯(NO2):向溶有杂质的硝基苯加入一定量的浓氢氧化钠溶液,振荡,分液可除去中溶解的NO2 |
分析 A.乙炔与酸性高锰酸钾反应生成二氧化碳气体;
B.苯酚与溴水反应生成三溴苯酚,三溴苯酚与苯互溶;
C.生石灰和水能反应;
D.氢氧化钠与NO2反应生成的硝酸钠和亚硝酸钠,溶于水,硝基苯不溶于水.
解答 解:A.乙炔与酸性高锰酸钾反应生成二氧化碳气体,引入新的杂质,应用溴水除杂,故A错误;
B.苯酚与溴水反应生成三溴苯酚,三溴苯酚与苯互溶,不能将杂质除去,且引入新的杂质,应加入氢氧化钠溶液然后分液,故B错误;
C.生石灰和水能反应生成氢氧化钙,所以生石灰能吸收蒸馏出的水分,从而制得无水酒精,故C正确;
D.氢氧化钠与NO2反应生成的硝酸钠和亚硝酸钠,溶于水,硝基苯不溶于水,振荡静置后分液,可除去,故D正确.
故选CD.
点评 本题综合考查物质的分离提纯的实验设计,侧重于化学知识的综合应用,题目难度中等,注意除杂时不能引入新的杂质.


科目:高中化学 来源: 题型:解答题
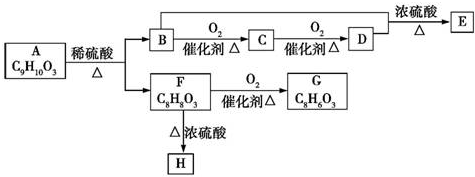
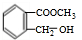 、
、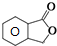 .
.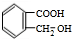 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2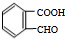 +2H2O.
+2H2O.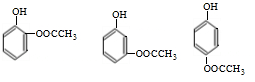 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
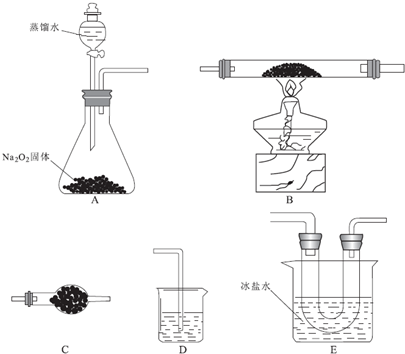
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10L | B. | 15L | C. | 25L | D. | 30L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水、浓H2SO4 | B. | 酸性KMnO4溶液、浓H2SO4 | ||
| C. | 溴水、浓H2SO4 | D. | CCl4、碱石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2气体通入Ba(NO3)2溶液中有白色沉淀生成 | |
| B. | 将足量的SO2气体通入Ba(OH)2溶液中有白色沉淀生成 | |
| C. | 将SO2气体通入BaCl2溶液中有白色沉淀生成 | |
| D. | 将Na2SO3与BaCl2溶液混合后生成白色沉淀,加稀硝酸沉淀全部溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
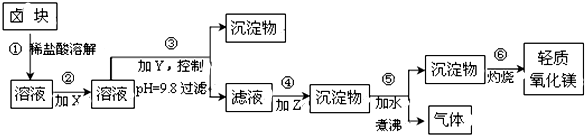
| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键存在于分子之间,也存在于分子之内 | |
| B. | 对于分子,其范德华力只随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 冰熔化时只破坏分子间作用力 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com