
| ||
| ||


科目:高中化学 来源: 题型:
 如图表示水溶液中c(H+)与c(OH-)的关系.
如图表示水溶液中c(H+)与c(OH-)的关系.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H2的电子式为H:C:::C:H |
| B、酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| C、鸡蛋白溶液中滴加饱和硫酸铵溶液,出现沉淀,该过程属于蛋白质的盐析 |
| D、6个碳原子形成的烃分子中,最多有5个碳碳单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和NaOH反应的中和热△H=2×(-57.3)kJ?mol-1 |
| B、CO的燃烧热是283kJ?mol-1,则2CO2(g)=2CO(g)+O2(g)△H=2×(+283)kJ?mol-1 |
| C、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下反应的△H不相同 |
| D、已知:2C(s)+2O2=2CO2(g)△H1,2C(s)+O2=2CO(g)△H2,则△H1>△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m1>m2 |
| B、m1≤m2 |
| C、m1≥m2 |
| D、m1=m2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、闪电时,空气中的氮气直接转化为二氧化氮 |
| B、实验室可用浓硫酸干燥二氧化硫 |
| C、不能用稀硝酸和活泼金属反应制氢气 |
| D、将足量二氧化硫通入酸性高锰酸钾试液中,溶液褪色说明二氧化硫具有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
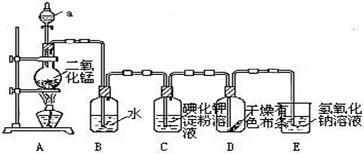
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7,c(SO42-)=c(NH4+) | ||
| B、两种醋酸溶液物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 | ||
| C、pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | ||
D、向0.1moL?L-1的氨水中加入少量硫酸铵固体,则溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com