
| A. | NaHS在水中的电离方程式为NaHS═Na++H++S2- | |
| B. | NaHS溶液水解的离子方程式为HS-+H2O═H2S↑+OH- | |
| C. | NaHS溶液与FeSO4溶液反应的离子方程式为S2-+Fe2+═FeS↓ | |
| D. | 向NaHS溶液中滴加过量的新制氯水:HS-+Cl2═S↓+H++2Cl- |
分析 A.电离生成氢离子和硫氢根离子;
B.水解为可逆反应;
C.硫氢根离子在离子反应中不能拆分;
D.发生氧化还原反应生成S、盐酸和氯化钠.
解答 解:A.NaHS在水中的电离方程式为NaHS═Na++HS-,故A错误;
B.NaHS溶液水解的离子方程式为HS-+H2O?H2S+OH-,故B错误;
C.NaHS溶液与FeSO4溶液反应的离子方程式为2HS-+Fe2+═FeS↓+2H+,故C错误;
D.向NaHS溶液中滴加过量的新制氯水的离子反应为HS-+Cl2═S↓+H++2Cl-,遵循电子、电荷守恒,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重电离、水解及氧化还原反应的离子反应考查,题目难度不大.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题

| A. | 淀粉尚有部分未水解 | |
| B. | 淀粉已完全水解 | |
| C. | 淀粉没有水解 | |
| D. | 淀粉已发生水解,但不知是否水解完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
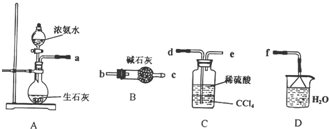
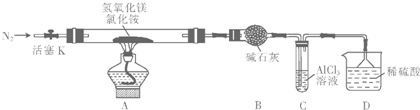
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
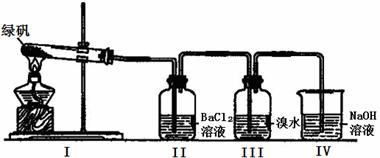
| 实验步骤 | 实验预期现象及结论 |
| 步骤一:取少量的FeSO4 固体于试管中,加入一定量水溶解 | |
| 步骤二: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
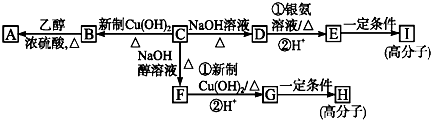
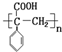 .
.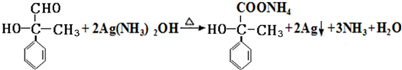 .
.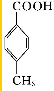 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧生成Na2O | |
| B. | 热稳定性,Na2CO3比NaHCO3强,而水溶性,NaHCO3 比Na2CO3易溶于水 | |
| C. | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明该溶液一定存在Na+,不存在K+ | |
| D. | 将Na投入NH4Cl溶液中可生成两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
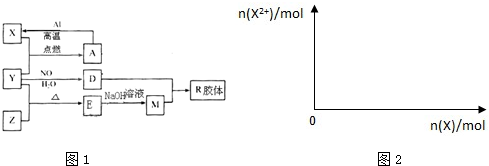
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com