
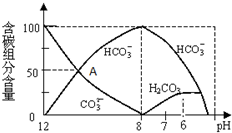
 常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示.回答下列问题:
常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示.回答下列问题:分析 (1)酸性条件下,能存在大量碳酸,碱性条件下,能存在大量碳酸根离子;
(2)常温下在20mL0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L HCl溶液40mL,先反应生成碳酸氢钠,再与盐酸反应生成二氧化碳、水,以此分析解答;
(3)OAB段碳酸氢根离子浓度增大,碳酸根离子浓度减小,说明碳酸根离子和氢离子反应生成碳酸氢根离子;当溶液中H2CO3达到饱和后,开始放出CO2气体.
解答 解:(1)H2CO3是二元弱酸,分步电离,电离方程式为:H2CO3?H++HCO3-,HCO3-?H++CO32-,HCO3-分别与H2CO3、CO32-都能共存,酸性条件下,能存在大量碳酸,碱性条件下,存在大量碳酸根离子,因为二者存在环境不同,所以H2CO3和CO32-在溶液中不能大量共存,
故答案为:不能;
(2)CO32-水解反应的平衡常数(即水解常数用Kh表示)Kn=$\frac{C(HC{O}_{3}^{-})•C(O{H}^{-})}{C(C{O}_{3}^{2-})}$=2×10-4,当溶液中c(HCO3-):c(CO32-)=2:1时,c(OH-)=10-4mol/L,由Kw可知,c(H+)=10-10mol/L,所以pH=10,
故答案为:10;
(3)Na2CO3溶液中加入少量盐酸生成HCO3-,反应的离子方程式为CO32-+H+=HCO3-,当溶液中H2CO3达到饱和后,开始放出CO2气体,由图象可以看出,当pH=6时,H2CO3达到饱和,开始放出CO2气体,
故答案为:6.
点评 本题考查溶液离子共存以及化学平衡常数的计算等问题,题目难度中等,注意分析图象曲线变化趋势,把握物质的性质,综合考查学生分析问题、解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率降低 | D. | C的体积分数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用铂丝做某溶液的焰色反应,火焰呈黄色 | 该溶液中一定含有钠盐 |
| B | 将二氧化硫通入到溴水中,溴水褪色 | 二氧化硫具有漂白性 |
| C | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去. | Na2CO3溶液中存在水解平衡 |
| D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com