
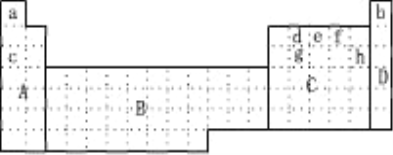
【题目】(1)下图所示元素周期表中全部是金属元素的区域为___________
A.A B.B C.C D.D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。______________
②甲、乙两元素相比较,金属性较强的是_________(填名称),可以验证该结论的实验是_______。
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出B的电子式:______,比较C、B、D结合氢离子的能力由强到弱的顺序为_________________(用化学式表示)。
(4)上表中c、h元素形成的简单离子半径之比________ 1(填〉或〈或 =)。
【答案】 B  镁 BC
镁 BC ![]() OH->NH3>H2O <
OH->NH3>H2O <
【解析】(1).B区为过渡元素区域,全部为金属元素,A区中H元素为非金属元素,C区中有大量非金属元素;
(2). 甲在冷的浓硫酸或空气中,表面都生成致密的氧化膜的是Al元素,乙为12号元素Mg,①Al元素位于ⅢA主族第三周期,Mg元素位于ⅡA主族第三周期;②Mg元素位于Al元素的左侧,则其金属性强;A. Al的表面会生成一层致密的氧化膜(Al2O3),防止了与水反应,Al2O3不溶于水,故不反应,MgO与水生成Mg(OH)2附着在表面,不与水反应,所以无法检验,A错误;B.根据气泡生成的多少克判断反应速率,进而判断金属性强弱,B正确;C. 依据最高价氧化物的水化物碱性的强弱。碱性越强,其元素的金属性越强,C正确;D.金属没有气态氢化物,D错误。故选择BC;
(3). 可以从常见的10电子微粒来分析判断:HF、OH-、H2O、NH3、H3O+、CH4、NH4+,则两个反应为:NH4++ OH-= NH3+ H2O,OH-+ H3O+=2 H2O,B为OH-,其电子式为: ![]() ;反应NH4++OH-=NH3·H2O,证明结合质子(H+)的能力OH->NH3,反应NH3+H3O+=NH4++H2O证明结合质子(H+)的能力NH3>H2O,可以确定OH-、NH3、H2O结合氢离子的能力为:OH->NH3>H2O;
;反应NH4++OH-=NH3·H2O,证明结合质子(H+)的能力OH->NH3,反应NH3+H3O+=NH4++H2O证明结合质子(H+)的能力NH3>H2O,可以确定OH-、NH3、H2O结合氢离子的能力为:OH->NH3>H2O;
(4). c、h元素分别为:Na和Cl,两者简单离子为Na+、Cl-,Cl-核外电子为3层,其半径大于Na+半径,故c、h简单离子半径之比小与1。


科目:高中化学 来源: 题型:
【题目】如图所示:在B水槽中装有500 mL水,容积为VL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B水槽的水中。充 分反应后,试管A中余下气体的体积为0.6VL。
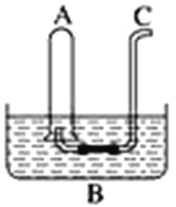
(1)将A倒插入B槽中发生的反应的化学方程为_________________,该反应中氧化剂与还原剂的质量比为________,原混合气体中NO2和NO的物质 的量之比为________。
(2)通过导气管C向余下0.6VL气体的试管A中持续通入氧气,A中可能观察到的现象是_________________________________
(3)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为________ mol·L-1(设溶液的体积仍为500 mL)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实行垃圾分类,关系生活环境改善和节约使用资源。下列说法正确的是
A.回收厨余垃圾用于提取食用油
B.对废油脂进行处理可获取氨基酸
C.回收旧报纸用于生产再生纸
D.废旧电池含重金属须深度填埋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年的新型冠状病毒中,口罩和医用酒精在防疫工作中起到重要作用,医用口罩由三层无纺布制成,无纺布的主要原料是聚丙烯树脂。下列说法正确的是( )
A.84消毒液、二氧化氯泡腾片可作环境消毒剂
B.聚丙烯树脂属于合成无机高分子材料
C.医用酒精中乙醇的体积分数为 95%
D.抗病毒疫苗冷藏存放的目的是避免蛋白质盐析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
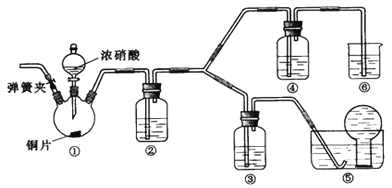
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应![]()
(1)装置①中发生反应的化学方程式是__________
(2)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹通入_________气体(填化学式)一段时间,关闭弹簧夹,将装置⑤中导管末端伸入倒置的烧瓶内。
(3)实验应避免有害气体排放到空气中,装置③中盛放的药品是_________;装置⑥中盛放的药品是_________。
(4)装置②中盛放的药品是_________;该装置的作用是_______________________。
(5)该小组得出的结论所依据的试验现象是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下除杂方法(括号内为少量杂质)中,错误的是( )
A.Fe(OH)3胶体(FeCl3溶液):蒸馏水,渗析
B.KCl(I2)固体:加热,升华
C.NaCl(KNO3):蒸发结晶
D.CO2(SO2):通过饱和NaHCO3溶液、浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.非极性分子只能是双原子单质分子
B.键能越大,表示该分子越容易受热分解
C.液态氟化氢中氟化氢分子之间存在氢键
D.分子中中心原子通过 sp3 杂化轨道成键时,该分子一定为正四面体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中,有A.B两种气体,反应按下式进行A(g)+B(g)═2C(g)反应经过2S后浓度不再发生变化时,测得容器中各物质的浓度分别为c(A)=0.5mol/L,c(B)=0.75mol/L,c(C)=0.5mol/L.
(1)B物质的起始浓度为
(2)2S时A的转化率
(3)用物质A表示反应的平均速率 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com