
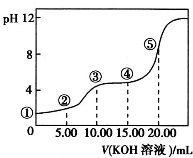
分析 (1)水的离子积只受温度影响,温度不变,水的离子积不变;
(2)根据溶液中存在的离子写出电荷守恒式;
(3)点③时两溶液恰好完全反应生成了KHC2O4,溶液显酸性,HC2O4-的电离程度大于水解程度;
(4)根据点④所示的溶液的体积25mL计算出溶液中各组分的浓度.
解答 解:(1)在任何的溶液中均存在水的离子积常数,室温下水的离子积为:KW=1×10-14,
故答案为:1×10-14;
(2)溶液中所有阳离子所带的正电荷总数一定等于阴离子所带的负电荷总数,即c(H+)+c(K+)=c(HC2O4-)+c(OH-)+2c(C2O42-),
故答案为:c(H+)+c(K+)=c(HC2O4-)+c(OH-)+2c(C2O42-);
(3)点③时两溶液恰好完全反应生成了KHC2O4,溶液显酸性,HC2O4-的电离程度大于水解程度,则溶液中离子浓度关系为:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
故答案为:c(K+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-);
(4)点④所示的溶液的体积25mL,根据物料守恒:c(HC2O4-)+c(H2C2O4)+c(C2O42-)=0.10mol/L×$\frac{10mL}{25mL}$=0.04mol/L;c(K+)=0.10mol/L×$\frac{15mL}{25mL}$=0.06mol/L,所以0.10mol•L-1=c(HC2O4-)+c(H2C2O4)+c(C2O42-)+c(K+),
故答案为:c(HC2O4-)+c(H2C2O4)+c(C2O42-)+c(K+).
点评 本题考查酸碱混合的定性判断及溶液pH的计算,题目难度中等,涉及中和滴定、物料守恒、电荷守恒等知识,试题知识点较多、综合性较强,解题时注意电荷守恒及物料守恒的应用,明确溶液酸碱性与溶液pH的关系为解答关键.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:填空题
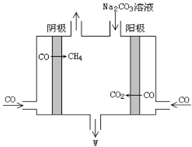 (1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O.
(1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
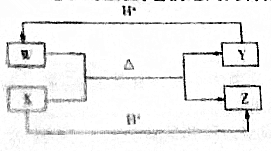
| A. | W的电子式为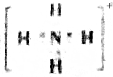 | |
| B. | Y与Z之间可形成氢键 | |
| C. | 硫酸与氢氧化钠溶液反应的离子方程式可表示为X+H+=Z | |
| D. | 微粒Y中各元素原子均达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原HA溶液中,c(H+)=c(A-) | |
| B. | 当恰好完全中和时,溶液呈中性 | |
| C. | 当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 当滴入少量的NaOH,促进了HA的电离,溶液的pH升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合液中由水电离出的c(H+)=1×10-8mol/L | |
| B. | c(A-)+c(HA)=2c(Na+)=0.4mol/L | |
| C. | HA溶液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$与混合液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$相等 | |
| D. | c(A-)-c(HA)=2c(OH-)-2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当V=10时,c(Na+)>c(OH-)>c(HC0${\;}_{3}^{-}$)>c(CH3COO-)>c(H+) | |
| B. | 当 0<V<20 时,c(H+)+c(Na+)=c(HC0${\;}_{3}^{-}$)+c(CH3COO-)+2 c(C032-)+c(OH-) | |
| C. | 当 V=20 时,c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 当 V=40 时,c(CH3COOH)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
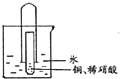 为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外.将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口.充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液.试回答:
为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加人适量稀硝酸,然后迅速将大试管倒扣在小试管外.将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口.充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴人几滴紫色石蕊试液.试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com