
分析 (1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,原子核外电子排布为1s22s22p3;
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,则乙为Cl元素、丙为K元素;
(3)丁元素的正三价离子的3d能级为半充满,原子核外电子排布式为1s22s22p63s23p63d64s2;
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子排布为1s22s22p63s23p63d104s1.
解答 解:(1)甲元素基态原子的最外层有3个未成对电子,次外层有2个电子,故为N元素,元素名称为氮;故原子核外电子排布为1s22s22p3,
故答案为:氮;1s22s22p3;
(2)乙元素的负一价离子和丙元素的正一价离子的电子层结构都与氩相同,则乙为Cl元素;丙为K元素,故原子核外电子排布为1s22s22p63s23p64s1,
故答案为:Cl;1s22s22p63s23p64s1;
(3)丁元素的正三价离子的3d能级为半充满,原子核外电子排布式为1s22s22p63s23p63d64s2;为Fe元素,
故答案为:Fe;1s22s22p63s23p63d64s2;
(4)戊元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,原子核外电子排布为1s22s22p63s23p63d104s1,元素在周期表中位置为:第四周期第ⅠB族,
故答案为:第四周期第ⅠB族;3d104s1.
点评 本题考查结构性质位置关系应用,侧重对核外电子排布规律的考查,难度不大,注意对基础知识的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的最简式:C6H6 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 2-乙基-1,3-丁二烯分子的键线式: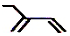 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
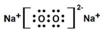
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
| B | 向稀硝酸中加入少量铁粉 | 有气泡产生 | 说明Fe置换出硝酸中的氢,生成了氢气 |
| C | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色胶状物质 | H2CO3的酸性比H2SiO3的酸性强 |
| D | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | NaHCO3为难溶物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 | 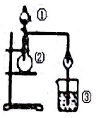 |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | Al2(SO4)3溶液 | Al(OH)3具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2C03 | Na2Si03 | 非金属性:C>Si |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
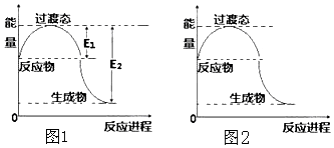 回答下列问题:
回答下列问题:| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能(kJ/mol) | 348 | 413 | 436 | 358 | 1072 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
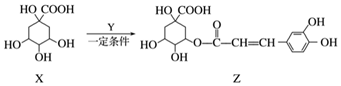
| A. | Z结构中有1个手性碳原子 | |
| B. | Y的分子式为C9H8O4 | |
| C. | 1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH | |
| D. | Z与浓溴水既能发生取代反应又能发生加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com