
【题目】向NaOH和Na2CO3混合溶液中滴加0.1 mol·L1稀盐酸,CO2的生成量与加入盐酸的体积的关系如图。下列判断正确的是
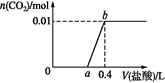
A. 在0~a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:![]()
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1∶2
【答案】C
【解析】
向氢氧化钠和碳酸钠的混合溶液中滴加盐酸,依次发生:H+和OH-的酸碱中和反应,H++CO32-=HCO3-,最后HCO3-+H+=H2O+CO2↑。生成的气体是0.01mol,所以碳酸氢根离子是0.01mol,根据碳守恒,Na2CO3为0.01mol。
A.在0~a范围内,除了发生酸碱中和,还发生H++CO32-=HCO3-,A错误;
B.ab段发生的反应是HCO3-+H+=H2O+CO2↑,B错误;
C. 0.01mol HCO3-消耗0.01mol H+,根据盐酸浓度0.1mol/L,从a到0.4消耗的盐酸为0.1L,所以a等于0.3,C正确;
D. a=0.3,在前两个反应中,共消耗0.03mol HCl,0.01mol Na2CO3消耗0.01mol HCl生成HCO3-,那么OH-消耗0.02mol H+,所以OH-为0.02mol,所以氢氧化钠和碳酸钠的物质的量之比是2:1,D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】(NH4)2SO4是一种常见的化肥,某工厂用石膏、NH3、H2O和CO2制备(NH4)2SO4的工艺流程如下:

下列说法正确的是
A. 通入NH3和CO2的顺序可以互换
B. 操作2为将滤液加热浓缩、冷却结晶、过滤,可得(NH4)2SO4
C. 步骤②中反应的离子方程式为Ca2++2NH3+CO2+H2O=CaCO3↓+2NH4+
D. 通入的NH2和CO2均应过量,且工艺流程中CO2可循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. H2SO4 和Ca(OH)2含有化学键类型相同
B. 水分子很稳定,是因为水分子的分子间作用力强
C. 二氧化碳和乙烯的碳原子的最外电子层都具有8电子稳定结构
D. 冰和水晶都是分子晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 向氯化铁溶液中加入过量的硫化钠:2Fe3++S2- = 2Fe2++S↓
B. 氢氧化铁溶于氢碘酸溶液:Fe(OH)3+ 3H+ = Fe3++ 3H2O
C. 硫酸铝溶液中加入过量氨水:Al3++ 4 NH3·H2O=AlO2- +4 NH![]() + 2 H2O
+ 2 H2O
D. 向NaHSO4溶液滴加Ba(OH)2溶液至中性:2H++SO42-+ Ba2++ 2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①写出乙炔的结构式________________;②写出水玻璃中溶质的化学式________________。
(2)写出二氧化锰与浓盐酸共热反应的化学方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在-50℃时液氨中存在着下列平衡:2NH3(液)![]() NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
A. 离子积为1.0×10-15
B. 离子积为1.0×10-30
C. 向液氨中加入氨基钠(NaNH2),液氨的离子积增大
D. 向液氨中加入NH4Cl,c(NH4+)增大,离子积的数值也随之增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列生物材料:①苹果②黄豆种子③梨④花生种子⑤蛋清⑥马铃薯块茎。最适于用来鉴定还原性糖的有 ( )
A. ①③⑥ B. ①②③ C. ①③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com