
 如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:
如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:| A. | 铁钉生锈,铁钉的腐蚀属于电化学腐蚀腐蚀 | |
| B. | 若试管内液面上升,则铁钉发生的是吸氧腐蚀 | |
| C. | 若试管内液面上升,则铁钉发生的是析氢腐蚀 | |
| D. | 若试管内液面下降,则铁钉发生的是析氢腐蚀 |
科目:高中化学 来源: 题型:选择题
| A. | X和Y能形成共价化合物 | |
| B. | Y与W形成的化合物Y2W2中含有离子键和共价键 | |
| C. | 简单离子的半径:Y>Z>W>X | |
| D. | 最高价氧化物对应水化物的酸性:Z>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高正价由低到高的顺序为:X、Z、Y、W | |
| B. | 原子半径由小到大的顺序为:X、Y、Z、W | |
| C. | 最外层电子数由少到多的顺序为:X、Z、Y、W | |
| D. | 简单氢化物的稳定性由弱到强的顺序为:Y、Z、W |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
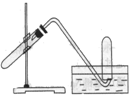
| A. | 加热NaHCO3制取和收集CO2 | |
| B. | 用铜和稀硝酸反应制取和收集NO | |
| C. | 用NH4Cl与浓NaOH溶液反应制取和收集NH3 | |
| D. | 用铜和浓硝酸反应制取和收集NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种不同元素的原子中,137Cs比131I多6个中子 | |
| B. | 多电子原子中,在离核较远的区域内运动的电子能量较低 | |
| C. | 同主族元素的简单阴离子还原性越强,其氢化物的稳定性越强 | |
| D. | 短周期元素X和Y的原子序数相差2,则X与Y可能同周期,也可能同主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=6的纯水中,c(OH-)=10-8 mol•L-1 | |
| B. | 向0.1 mol•L-1Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| C. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后溶液pH>7 | |
| D. | 0.1 mol•L-1Na2CO3溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
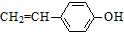 )常用于肉香和海鲜香精配方中.
)常用于肉香和海鲜香精配方中.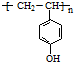 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com