

| A. | 电极X上发生氧化反应 | |
| B. | 电极Y上有气体产生 | |
| C. | 接通电路时,电子从电源的负极流出经过溶液后再从正极流 回电源 | |
| D. | 若反应中有0.1mol电子转移则阴极产物的质量为3.2g |
分析 A.连接电源负极的为阴极;
B.电极Y为阳极,发生的电极反应方程式为2Cl--2e-=Cl2↑;
C.电子流行负极→阴极→溶液→阳极→正极;
D.阴极发生的电极反应方程式为Cu2++2e-=Cu,据此进行计算.
解答 解:A.连接电源负极的为阴极,阴极发生还原反应,故A错误;
B.电极Y为阳极,发生的电极反应方程式为2Cl--2e-=Cl2↑,故电极Y上有气体产生,故B正确;
C.电子流行负极→阴极→溶液→阳极→正极,故C错误;
D.阴极发生的电极反应方程式为Cu2++2e-=Cu,
2 64
0.1 3.2,故阴极产物的质量为3.2g,故D正确,
故选BD.
点评 本题考查了电解池的反应原理的应用,电子流向、电极判断,阴极质量的变化,题目较简单.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:选择题

| A. | 该检测仪利用了电解原理 | |
| B. | 质子交换膜具有类似盐桥的平衡电荷作用 | |
| C. | Pt(l)极反应为:CH3CH2OH-4e-+H2O=4H++CH3COOH | |
| D. | 工作中电子由Pt(l)电极经过质子交换膜流向Pt(II) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在CH2=CH2分子中,存在4个σ键和一个π键 | |
| B. | 在共价化合物中,一定存在极性键,可能存在非极性键,一定不存在离子键 | |
| C. | N、O、F电负性大小:F>O>N;第一电离能大小:F>O>N | |
| D. | 酸性强弱:H2SO4>H2SO3>H2SeO3;岩浆晶出的先后顺序:SiO2、MgSiO3、CaSiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
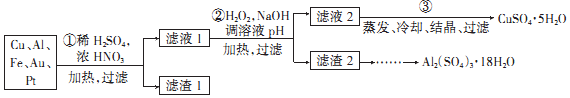
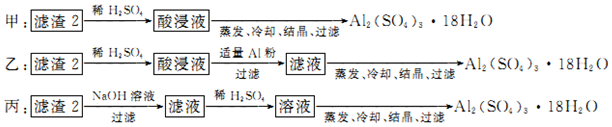
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
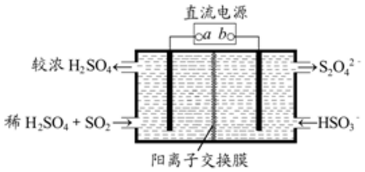 利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )
利用如图所示装置(电极均为惰性电极)可吸收SO2,并用阴极排出的溶液可吸收NO2.下列说法正确的是( )| A. | a为直流电源的负极 | |
| B. | 与 b电极相连的电极反应式为:2HSO3-+2H++2e-═S2O42-+2H2O | |
| C. | 与 a相连的电极发生还原反应得到SO42- | |
| D. | 电解时,H+由阴极室通过阳离子交换膜到阳极室 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③①⑤ | B. | ②③⑤① | C. | ④⑥③① | D. | ④⑤⑥③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是
乙酸橙花酯兼有橙花和玫瑰花香气,其结构简式如图.关于该有机物的叙述中正确的是| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑤ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 0.1 mol丙烯酸(CH2=CHCOOH)中含有碳原子的数目为0.2NA | |
| C. | 标准状况下,11.2LCCl4中含有分子的数目为0.5NA | |
| D. | 在2Na2O2+2H2O═4NaOH+O2↑的反应中,每生成0.1 mol氧气,转移电子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7 | |
| B. | 钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能 | |
| C. | 高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性 | |
| D. | 邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com