
【题目】干冰、石墨、C60、氟化钙和金刚石的结构模型如图所示(石墨仅表示出其中的一层结构):

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________。
(4)在CaF2晶体中,Ca2+的配位数是________,F-的配位数是________。
(5)固态时,C60属于________ (填“原子”或“分子”)晶体。
【答案】12 8 2 8 4 分子
【解析】
根据各种晶胞的结构进行分析判断;
(1)干冰是分子晶体, CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在与该顶点相连的12个面的面心上,所以干冰晶胞中,每个CO2分子周围有12个与之紧邻且等距的CO2分子;因此,本题正确答案是:12;
(2)金刚石晶胞中碳原子占据立方体的面心和顶点,晶胞内部有4个碳原子,则每个金刚石晶胞占有碳原子数为:![]() +
+![]() 6+4=8,因此,本题正确答案是:8;
6+4=8,因此,本题正确答案是:8;
(3)石墨层状结构中,每个碳原子被三个正六边形共用,所以平均每个正六边形占有的碳原子数=6×![]() =2;答案:2。
=2;答案:2。
(4)在CaF2晶胞中每个Ca2+连接4个氟离子,但在下面一个晶胞中又连接4个氟离子,即每个Ca位于8个F构成的立方体体心,所以其配位数为8;同理每个F均位于四个Ca2+构成的正四面体的体心,所以其配位数为4,因此,本题正确答案是:8;4;
(5)C60中构成微粒是分子,所以属于分子晶体;答案:分子。


科目:高中化学 来源: 题型:
【题目】有机物A只由C、H、O三种元素组成,常用作有机合成的中间体,测得8.4g该有机物经燃烧生成22.0g CO2和7.2g水,质谱图表明其相对分子质量为84;红外光谱分析表明A中含有-OH和位于分子端的-C≡C-,核磁共振氢谱显示有3种峰,且峰面积之比为6:1:1。试通过计算求A的分子式和结构简式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫力功能的药物,可通过以下方法合成:

(1)物质A的名称是__________________________
(2)B→C的转化属于_______反应(填反应类型)。
(3)上述流程中设计A→B步骤的目的是_________________________________。
(4)A与足量氢氧化钠溶液反应的方程式为:_________________________________。
(5)A的同分异构体X满足下列条件:
Ⅰ.能与NaHCO3反应放出气体; Ⅱ.能与FeCl3溶液发生显色反应。
符合上述条件的同分异构体有______种。其中核磁共振氢谱有5组吸收峰的结构简式为_____________。
(6)参照上述合成路线和信息,以乙醛为原料(无机试剂任选),设计制
的合成路线:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化在给定条件下不能实现的是
A. Fe2O3![]() FeCl3(aq)
FeCl3(aq) ![]() 无水FeCl3
无水FeCl3
B. Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq) ![]() AlCl3(aq)
AlCl3(aq)
C. NH3![]() NO
NO![]() HNO3
HNO3
D. SiO2![]() H2SiO3
H2SiO3![]() Na2SiO3
Na2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为_________________________,第一电离能介于N和B之间的第二周期元素有_______种。
(2)HCN分子中σ键与π键的数目之比为_______,其中σ键的对称方式为___________。与CN—互为等电子体的分子为___________。
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子中心原子的杂化轨道类型为_________。NF3的空间构型为____________。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如下表所示,分析其变化原因_________________________________________________________。
GaN | GaP | GaAs | |
熔点 | 1700℃ | 1480℃ | 1238℃ |
(5)GaN晶胞结构如下图所示。已知六棱柱底边边长为a cm,阿伏加德罗常数的值为NA。


① 晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_____________;
② GaN的密度为______________________g·cm3(用a、NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① NO + NO2 + 2NaOH![]() 2NaNO2 + H2O;
2NaNO2 + H2O;
② 2NO2 + 2NaOH![]() NaNO3 + NaNO2 + H2O
NaNO3 + NaNO2 + H2O
将51.2 g Cu溶于一定浓度的硝酸中,若生成的气体只含有NO、NO2,且这些气体恰好被500 mL2.0 mol/L的NaOH溶液完全吸收,得到只含NaNO2和NaNO3的溶液。求:气体中NO、NO2的物质的量分别为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物能形成酸雨和光化学烟雾,严重污染环境。燃煤和机动车尾气是氮氧化物的主要来源。现在对其中的一些气体进行了一定的研究:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) △H= 574 kJ·moll
4NO(g)+CO2(g)+2H2O(g) △H= 574 kJ·moll
②CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) △H= 1160 kJ·moll
2N2(g)+CO2(g)+2H2O(g) △H= 1160 kJ·moll
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(g)的热化学方程式______________________________________________________。
(2)在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体。T℃时,将等物质的量的NO和CO充入容积为2 L的密闭容器中,保持温度和体积不变,在一定条件下发生反应,反应过程中NO的物质的量随时间变化如图所示。
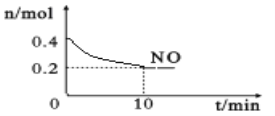
①写出该反应的化学方程式______________________________________。
②10 min内该反应的速率v(CO)=__________________;T℃时,该化学反应的平衡常数K=_______。
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________。(填序号)
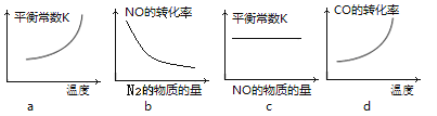
④一定温度下,在恒容密闭容器中充入一定量NO和CO进行该反应,下列选项能判断反应已达到化学平衡状态的是____________。
A.容器中压强不再变化 B.混合气体的平均相对分子质量不再变化
C.2v正(NO)=v逆(N2) D.气体的密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明苯酚具有弱酸性的实验是( )
A.加入浓溴水生成白色沉淀
B.苯酚的水溶液中加 NaOH溶液,生成苯酚钠
C.苯酚的浑浊液加热后变澄清
D.苯酚钠溶液中通入CO2后,溶液由澄清变浑浊
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com