
| A. | [A-]=[K+] | B. | [H+]=[OH-]<[K+]<[A-] | C. | V总≥30mL | D. | V总≤30mL |
分析 pH=11的KOH溶液,c(OH-)=0.001mol/L,pH=3的一元酸HA溶液若强酸,c(H+)=c(HA)=0.001mol/L,混合后pH=7,则等体积混合;
若酸为弱酸,c(HA)>0.001mol/L,混合后pH=7时,应为醋酸和醋酸钾的混合溶液,其体积应小于15mL,以此来解答.
解答 解:pH=11的KOH溶液,c(OH-)=0.001mol/L,pH=3的一元酸HA溶液若强酸,c(H+)=c(HA)=0.001mol/L,混合后pH=7,则等体积混合;
若酸为弱酸,c(HA)>0.001mol/L,混合后pH=7时,应为醋酸和醋酸钾的混合溶液,其体积应小于15mL,即V总≤30mL,
又pH=7,则c(OH-)=c(H+),由电荷守恒可知,c(H+)+c(K+)=c(OH-)+c(A-),则c(A-)=c(K+),
溶液中显性离子浓度大于隐性离子浓度,所以c(A-)=c(K+)>c(OH-)=c(H+),
故选AD.
点评 本题考查酸碱混合溶液的计算,明确酸的强弱及电荷守恒是解答本题的关键,注意酸为弱酸时浓度大,其体积应小于碱的体积才能满足混合溶液的pH=7,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CO32-、H+、NO3-、Na+ | B. | OH-、K+、NO3-、Cl- | ||
| C. | Mg2+、H+、OH-、SO42- | D. | Na+、Cu2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ||||||
| 4 | ⑧ | ⑨ | ||||||
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做过KMn04分解反应实验的试管(浓盐酸) | |
| B. | 做过木炭还原氧化铜实验的试管(硝酸) | |
| C. | 做过银镜反应实验的试管(氨水) | |
| D. | 做过Na2S2O3与稀硫酸反应的试管(二硫化碳) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
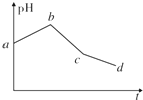 将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )
将物质的量浓度相等的KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如上图所示,则下列说法正确的是( )| A. | ab段表示电解过程中H+被还原,pH上升 | |
| B. | 电解开始时阳极先发生电极反应2Cl--2e-═Cl2↑ | |
| C. | 电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度 | |
| D. | 原混合溶液中KCl和CuSO4的浓度之比恰好为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何条件下,纯水都呈中性 | |
| B. | 电离平衡常数Ka越小,表示弱电解质电离能力越强 | |
| C. | 为保存FeCl3溶液,要在溶液中加少量硫酸 | |
| D. | 明矾溶液蒸干得到的固体为Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol任何物质的体积为22.4L | |
| B. | 等物质的量的HCl和 H 2 SO4中,H+的物质的量也相等 | |
| C. | 1molH 2和1molHe中,所含的分子数相同、原子数相同、质量也相同 | |
| D. | 体积为6L的 O 2,其质量可能为8g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com