
����Ŀ��A��B��C��D��E��F��G��Ϊ������Ԫ�أ�ԭ���������ε�����AԪ��ԭ�Ӻ��������ӣ�BԪ��ԭ�������������Ǵ�����������2����D�ǵؿ��к�������Ԫ�أ�E�Ƕ������н�������ǿ��Ԫ�أ�F��Gλ�����ڣ�G��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ���ش��������⣨��ӦԪ�ؾ���Ԫ�ط��ű�ʾ����
��1��C��Ԫ�����ڱ��е�λ��Ϊ �� G��ԭ�ӽṹʾ��ͼ�� ��
��2��D��E��ԭ�Ӹ�����1��1�γɻ�����ף������ʽΪ �� ������ѧ������Ϊ ��
��3������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�� ��
��4��E��F��G����Ԫ�����γɵļ����ӣ��뾶�ɴ�С��˳���� ��
��5����BA4��D2��EDA��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��BA4���壬b��ͨ��D2���壬��a���Ǹõ�ص����������ĵ缫��ӦʽΪ ��
���𰸡�
��1���ڶ����ڵ�VA�壻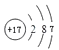
��2��![]() �����Ӽ������ۼ�
�����Ӽ������ۼ�
��3��2Na2O2+2H2O�T4NaOH+O2��
��4��S2����Cl����Na+
��5��������O2+2H2O+4e���T4OH��
���������⣺A��B��C��D��E��F��G��Ϊ������Ԫ�أ�ԭ���������ε�����AԪ��ԭ�Ӻ��������ӣ���AΪ��Ԫ�أ�BԪ��ԭ�Ӻ��������������Ǵ�����������2������B��2�����Ӳ㣬�������4�����ӣ���BΪ̼Ԫ�أ�DԪ���ǵؿ��к�������Ԫ�أ���DΪ��Ԫ�أ�Cԭ����������̼����֮�䣬��CΪ��Ԫ�أ�EԪ���Ƕ�����Ԫ���н�������ǿ��Ԫ�أ���EΪNa��F��G��λ�����ڣ�G��ͬ����Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�����֪FΪSԪ�ء�GΪClԪ�أ���1��C�ǵ�Ԫ�أ�ԭ����2�����Ӳ㣬����������Ϊ5����Ԫ�����ڱ��е�λ�ã��ڶ����ڵ�VA�壬GΪClԪ�أ�ԭ�ӽṹʾ��ͼ��  �����Դ��ǣ��ڶ����ڵ�VA�壻
�����Դ��ǣ��ڶ����ڵ�VA�壻  ����2��D��E��ԭ�Ӹ�����1��1�γɻ������ΪNa2O2 �� �����ʽΪ
����2��D��E��ԭ�Ӹ�����1��1�γɻ������ΪNa2O2 �� �����ʽΪ ![]() ��������ѧ������Ϊ�����Ӽ������ۼ������Դ��ǣ�
��������ѧ������Ϊ�����Ӽ������ۼ������Դ��ǣ� ![]() �����Ӽ������ۼ�����3������������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2H2O�T4NaOH+O2�������Դ��ǣ�2Na2O2+2H2O�T4NaOH+O2������4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶�ɴ�С��˳���ǣ�S2����Cl����Na+ �� ���Դ��ǣ�S2����Cl����Na+����5����CH4��O2��NaOH��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��CH4���壬b��ͨ��O2���壬���鷢��������Ӧ����a���Ǹõ�صĸ�����bΪ������������������õ��ӣ������������������������ӣ������ĵ缫��ӦʽΪ��O2+2H2O+4e���T4OH�� �� ���Դ��ǣ�����O2+2H2O+4e���T4OH�� ��
�����Ӽ������ۼ�����3������������еμ�����ˮʱ������Ӧ�Ļ�ѧ����ʽ�ǣ�2Na2O2+2H2O�T4NaOH+O2�������Դ��ǣ�2Na2O2+2H2O�T4NaOH+O2������4�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶�ɴ�С��˳���ǣ�S2����Cl����Na+ �� ���Դ��ǣ�S2����Cl����Na+����5����CH4��O2��NaOH��ˮ��Һ���ȼ�ϵ�أ��缫����Ϊ����Խ����缫����a��ͨ��CH4���壬b��ͨ��O2���壬���鷢��������Ӧ����a���Ǹõ�صĸ�����bΪ������������������õ��ӣ������������������������ӣ������ĵ缫��ӦʽΪ��O2+2H2O+4e���T4OH�� �� ���Դ��ǣ�����O2+2H2O+4e���T4OH�� ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ȤС���ijƷ��������Ħ�����ɷּ��京����������̽����
������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ�����������
��1��Ħ���������������Ķ��Լ��飮
ȡ����������Ʒ����ˮ��ֽ��衢���ˣ�
�������м������NaOH��Һ�����ˣ���Һ��ͨ�����������̼����д��ͨ�����������̼��Ӧ�����ӷ���ʽ�� ��
��2��������Ʒ��̼��ƵĶ����ⶨ��
������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������
����ʵ����̻ش��������⣺
��i��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬����
��ii��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��
��iii�����и����ʩ�У�������߲ⶨȷ�ȵ��������ţ���
a���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2����
b���μ�����˹���
c����A��B֮������ʢ��Ũ�����ϴ��װ��
d����B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
��iv��ʵ����ȷ��ȡ8.00g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94g������Ʒ��̼��Ƶ���������Ϊ
��v��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ���������Ϳ���ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶�ʱ����1mol A��2mol B�����ݻ�Ϊ5L��ij�ܱ������з������·�Ӧ��A��s��+2B��g��C��g��+2D��g������5min���������B���ʵ�Ũ�ȼ�����0.2molL��1 �� ������������ȷ���ǣ� ��
A.��5min�ڸ÷�Ӧ��C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.02molL��1min��1
B.��5minʱ��������D��Ũ��Ϊ0.2molL��1
C.�÷�Ӧ���ŷ�Ӧ�Ľ��У�������ѹǿ������
D.5minʱ�����������ܵ����ʵ���Ϊ3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������þ����������Һ�������Ϻ�������Ũ��Ϊ0.1mol��L-1����������ӵ�Ũ��Ϊ0.3mol��L-1������Һ��þ���ӵ�Ũ��Ϊ
A. 0��15mol��L-1 B. 0��3mol��L-1 C. 0��45mol��L-1 D. 0��2mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijģ�⡰�˹���Ҷ���绯ѧʵ��װ����ͼ��ʾ����װ���ܽ�H2O��CO2ת��ΪO2��ȼ�ϣ�C3H8O��������˵����ȷ���ǣ� �� 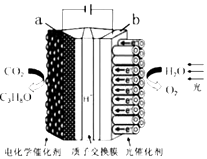
A.a�缫�ķ�ӦΪ��3CO2+18H++18e��=C3H8O+5H2O
B.��װ�ù���ʱ��H+��b������a����Ǩ��
C.ÿ����1molO2 �� ��44gCO2����ԭ
D.��װ�ý���ѧ��ת��Ϊ���ܺ͵���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������ʱ��ɫ��ӦΪ��ɫ���������ж���ȷ����( )
A. ������һ�����ƵĻ�����
B. ������һ���ǽ�����
C. ������һ�����Ȼ���
D. ������һ������Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ���õ����ز�����ͭ��װ��ͼ��ʾ�˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4������˵������ȷ����

A. �ù����ǽ�̫����ת��Ϊ��ѧ�ܵĹ���
B. GaN���淢��������Ӧ��2H2O��4 e��=== O2����4H��
C. Cu����ķ�Ӧ�ǣ�CO2��8e����6H2O === CH4��8OH
D. H+�����ӽ���Ĥ��������Ǩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е��뷽��ʽ����ȷ���ǣ� ��
A.NaHSO4����ˮ��NaHSO4Na++H++SO42��
B.��������룺HClO�TClO��+H+
C.HF����ˮ��HF+H2OH3O++F��
D.NH4Cl����ˮ��NH4++H2ONH3H2O+H+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com