
| A. | 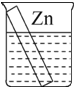 | B. | 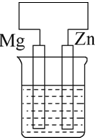 | C. | 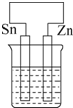 | D. | 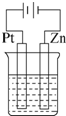 |
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:填空题
 烟气脱硫(SO2)脱硝(NOx)一体化技术是大气污染防治研究的热点.烟气中NO通常占NOx总量的90%以上,但NO的脱除难度较大.某研究小组探究用次氯酸钙溶液同时脱除烟气中SO2和NO的方法.
烟气脱硫(SO2)脱硝(NOx)一体化技术是大气污染防治研究的热点.烟气中NO通常占NOx总量的90%以上,但NO的脱除难度较大.某研究小组探究用次氯酸钙溶液同时脱除烟气中SO2和NO的方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肯定有O2和NO | B. | 肯定没有Cl2、O2和NO2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol•L-1CH3COONa溶液和0.1 mol•L-1HCl溶液等体积混合后:c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-) | |
| B. | pH=3的盐酸和NaOH的混合溶液中:c(Na+)=c(Cl-) | |
| C. | 0.1 mol•L-1NaHCO3 溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| D. | 含SO42-、NH4+、H+、OH-的溶液中可能存在:c(H+)>c(SO42-)>c(NH4+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的正极板上覆盖有PbO2,负极板上覆盖有Pb | |
| B. | 该电池放电时的正极反应为PbO2(s)+4H+(aq)+SO2-4(aq)+2e-═PbSO4(s)+2H2O(l) | |
| C. | 该电池充电时,两个电极上都有PbSO4生成 | |
| D. | 用该电池电解饱和食盐水制氯气,若制得0.050molCl2,这时电池内消耗H2SO40.10mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制100mL2mol/LNaCl溶液,将称量的NaCl放入烧杯中加20-30mL的蒸馏水搅拌溶解 | |
| B. | 蒸馏操作时,应将温度计插入烧瓶中的溶液中 | |
| C. | 测溶液的pH时,将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 | |
| D. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
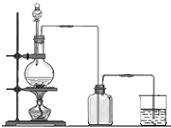 实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答:
实验室用MnO2和浓盐酸反应制取Cl2,气体发生和收集装置如图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打是面包发酵粉的主要成分之一 | |
| B. | 碳酸钠可作胃酸的中和剂 | |
| C. | “血液透析”利用了胶体的性质 | |
| D. | 利用明矾溶液的酸性清除铜镜表面的铜锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com