
| A. | Na+、Cl-、Br-、I- | B. | Ba2+、Na+、Cl-、SO42- | ||
| C. | Al3+、K+、HCO3-、Cl- | D. | Na+、K+、Ag+、NO3- |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应、不能发生相互促进水解反应等,则离子大量共存,以此来解答.
解答 解:A.该组离子与盐酸或NaOH均不反应,可大量共存,故A选;
B.Ba2+、SO42-结合生成沉淀,不能共存,故B不选;
C.Al3+、HCO3-相互促进水解,Al3+、HCO3-均与NaOH反应,HCO3-与HCl反应,不能共存,故C不选;
D.加盐酸或NaOH时Ag+、Cl-(或OH-)结合生成沉淀,不能共存,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
 如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH$?_{充电}^{放电}$2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH$?_{充电}^{放电}$2K2CO3+6H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ①⑥⑨ | C. | ①⑧ | D. | ①②⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K3[Fe(SCN)6] | B. | [Cu(NH3)4]Cl2 | C. | Na3[AlF6] | D. | Na2[SiF6] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部可以 | B. | 仅②可以 | C. | 仅②⑤可以 | D. | ①③④可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L NH4Al(SO4)2溶液中离子浓度大小关系为c(SO42-)>c(Al3+)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1 mol•L-1 HA(一元酸)溶液与0.1 mol•L-1的NaOH溶液等体积混合:c(H+)+c(Na+)═c(OH-)+c(A-) | |
| C. | 将0.1 mol/L的醋酸溶液加水稀释的过程中,溶液里所有离子浓度都减小 | |
| D. | 向CaSO4和BaSO4沉淀共存的体系中加入少量BaCl2,溶液中c(Ca2+)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
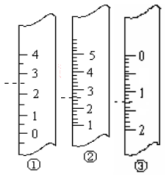 (1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是①,读数是2.5℃,量筒应该是②,读数为2.5 mL,滴定管应该是③,读数为1.30 mL
(1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是①,读数是2.5℃,量筒应该是②,读数为2.5 mL,滴定管应该是③,读数为1.30 mL查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com