
| 熔点/℃ | 沸点/℃ | 密度/g•mL-1 | 其他 | |
| 黄磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl3 2P+5Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2PCl5 |
| PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |

分析 (一)(1)仪器乙名称从装置中分析为冷凝管;冷凝管采用逆向通水法的冷凝效果较好;
(2)漂白粉有效成分为次氯酸钙,次氯酸钙与盐酸反应生成氯气、氯化钙和水,据此写出反应的化学方程式;
(3)碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度;
(4)由于PCl3遇O2会生成POCl3,遇水生成H3PO3和HCl,通入一段时间的CO2可以排尽装置中的空气,防止生成的PCl3与空气中的O2和水反应;通入二氧化碳赶净空气,避免水和氧气与三氯化磷发生反应;
(二)(5)依据物质的沸点数值不同,可以利用蒸馏的方法分离出三氯化磷;
(三)(6)依据反应的化学方程式H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6 计算,注意溶液体积的变化;
解答 解:(一)(1)仪器乙为冷凝管,用于冷凝蒸馏产物;冷凝管中通水方向为逆向,即从b通水,
故答案为:冷凝管;b;
(2)漂白粉和浓盐酸发生反应生成氯气的化学反应为:Ca(ClO)2+4HCl(浓)=CaCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(3)氯气有毒,污染空气,碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度,
故答案为:碱石灰吸收多余氯气防止污染空气,防止空气中的水蒸气进入影响产品纯度;
(4)由于PCl3遇O2会生成POCl3,遇水生成H3PO3和HCl,通入一段时间的CO2可以排尽装置中的空气,防止生成的PCl3与空气中的O2和水反应;通入二氧化碳赶净空气,避免水和氧气与三氯化磷发生反应,
故答案为:排净装置中的空气,防止空气中的水分和氧气与PCl3反应;
(二)(5)依据物质的沸点数值不同,可以利用蒸馏的方法分离出三氯化磷,
故答为:蒸馏;
(三)(6)0.1000mol•L-1碘溶液23.00mL中含有碘单质的物质的量为:0.1000mol•L-1×0.023L=0.0023mol,根据反应I2+2Na2S2O3=2NaI+Na2S4O6可知,与磷酸反应消耗的碘单质的物质的量为:0.0023mol-0.1000mol•L-1×0.01L×$\frac{1}{2}$=0.0018mol,再由H3PO3+H2O+I2=H3PO4+2HI可知,25mL三氯化磷水解后的溶液中含有的H3PO3的物质的量为:n(H3PO3)=n(I2)=0.0018mol,500mL该溶液中含有H3PO3的物质的量为:0.0018mol×$\frac{500mL}{25mL}$=0.036mol,所以5.500g产品中含有的三氯化磷的物质的量为0.036mol,该产品中PCl3的质量分数为:$\frac{137.5g/mol×0.036mol}{5.5g}$×100%≈90.0%,
故答案为:90.0%.
点评 本题考查物质组成与含量的测定、对实验原理理解、氧化还原滴定、阅读获取信息的能力等,难度较大,是对知识的综合运用,理解实验原理是解题的关键,需要学生具有扎实的基础与综合运用分析解决问题的能力,质量分数计算量较大、步骤较多,是易错点.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{500a}{23V}$mol/L | B. | $\frac{142a}{46V}$mol/L | C. | $\frac{142a}{23V}$mol/L | D. | $\frac{1000a}{23V}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖的结构简式:C6H12O6 | B. | 乙烯的结构简式:CH2=CH2 | ||
| C. | 甲烷分子的比例模型: | D. | Cl-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
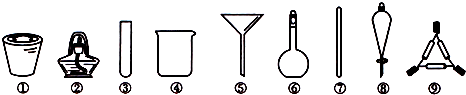
| A. | 将海带高温灼烧,选用①、②、⑨ | |
| B. | 过滤粗盐水,选用④、⑤、⑦ | |
| C. | 四氯化碳萃取溴水中的溴,选用④、⑥、⑧ | |
| D. | 加热碳酸氢钠固体并检验其产物,选用②、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、需要加热才能进行的化学反应一定是吸热反应 | |
| B. | 化学反应中的能量变化除了热量外还可以是光能、电能等 | |
| C. | 化学反应过程中的能量变化服从能量守恒定律 | |
| D. | 生成物的总能量小于反应物的总能量时发生的是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g羟基(-OH)所含有的电子数是NA | |
| B. | 常温常压下,4g氮气所含有的原子数目为NA | |
| C. | 1 L 0.1mol•L-1乙酸溶液中H+数为0.1NA | |
| D. | 标准状况下,22.4L乙醇的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com