
����Ŀ�����Ϳ����������Ӽ�ͨ��ʹ��1��2-�������飬������������ɫҺ�壬�ܶ�2.18 g��cm-3���е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�������ͼ��ʾװ���Ʊ�1��2-�������顣���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Һ�壨���渲������ˮ������д���пհף�
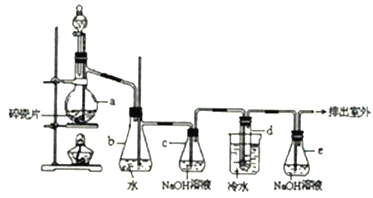
��1��װ��a�����Ƭ��������__________________________��
��2����ȫƿb���Է�ֹ�����������Լ��ʵ�����ʱ�Թ�d�Ƿ�����������д����������ʱƿb�е�����______________________��
��3���жϸ��Ʊ���Ӧ������������ķ�����________________________________��
��4��д��װ��e�з����ķ�Ӧ�����ӷ���ʽ_______________________________��
��5����1��2����������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ�� _____________�㣨��ϡ������¡�������������������δ��Ӧ��Br2�������_______________ϴ�ӳ�ȥ������ȷѡ��ǰ����ĸ����
a��ˮ b������������Һ c���⻯����Һ d���Ҵ�
��6��ʵ�����ʱ���Ƶô�����1��2-��������18.8g�������������Ҵ�_______________g��
��7��ijѧ��������ʵ��ʱʹ����һ������Һ�壬����Ӧ����ʱ�����������Ҵ���������������³������ࡣԭ�����װ�õ������Բ���֮�⣬���п��ܵ�2��ԭ��_______________��_______________��
���𰸡� ��ֹ���� b��ˮ����½����������е�ˮ����������������� �����ɫ��ȫ��ȥ 2OH-+Br2=Br-+BrO-��H2O �� b 4.6 ��ϩ��������ͨ��Һ�壩�ٶȹ��� ʵ������У��Ҵ���Ũ����Ļ��Һû��Ѹ�ٴﵽ170�棨��"���²���"��ɣ�
���������Ҵ���Ũ���ᷴӦ��Ҫ������ϩ���壬Ũ������ǿ�����Ժ���ˮ�ԣ����Ի����ܻ���̼��Ũ���ᷴӦ���ɵ�CO2��SO2���壬bΪ��ȫƿ��cΪ��������װ�ã�dΪ��ϩ����ķ�Ӧװ�ã�eΪβ������װ�á�
(1)װ��a�����Ƭ���Է�ֹҺ�����ʱ�������У��ʴ�Ϊ����ֹ���У�
(2)�Թ�d��������ʱ��b��ѹǿ�������ᵼ��b��ˮ���½����������е�ˮ������������������ʴ�Ϊ��b��ˮ����½����������е�ˮ������������������
(3)�жϸ��Ʊ���Ӧ�Ѿ�������������ǣ���ϩ����ˮ�����ӳɷ�Ӧ����1��2-�������飬1��2-��������Ϊ��ɫ�������жϷ�Ӧ�����ķ����ǹ۲�d����ˮ��ȫ��ɫ���ʴ�Ϊ����ˮ��ɫ��ȫ��ȥ��
(4)װ��e������β������ֹ����Ⱦ��������Ӧ�����ӷ���ʽΪ2OH-+Br2=Br-+BrO-��H2O���ʴ�Ϊ��2OH-+Br2=Br-+BrO-��H2O��
(5)1��2������������ܶȱ�ˮ���ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ���²㣬��������������δ��Ӧ��Br2�����������������Һ���廹ԭΪ����ˮ���廯��ϴ�ӳ�ȥ������ˮ�е��ܽ�Ȳ����ܺܺõij�ȥ����⻯�Ʒ�Ӧ���ɵ⣬�����������ʵ⣬���߾��������Ҵ����������Ҵ����ӣ��ʴ�Ϊ���£�b��
(6)����C2H5OH~C2H4~C2H4Br2��18.8g1��2-������������ʵ���Ϊ![]() =0.1mol������Ҫ�Ҵ�������Ϊ0.1mol��46g/mol=4.6g���ʴ�Ϊ��4.6��
=0.1mol������Ҫ�Ҵ�������Ϊ0.1mol��46g/mol=4.6g���ʴ�Ϊ��4.6��
(7)��Ӧ����ʱ�����������Ҵ���������������³������࣬���ܵ�ԭ�����װ�õ������Բ���֮�⣬���п�������ϩ����ͨ��Һ����ٶȹ��졢ʵ������У��Ҵ���Ũ����Ļ��Һû��Ѹ�ٴﵽ170��ȣ��ʴ�Ϊ����ϩ����ͨ��Һ����ٶȹ��졢ʵ������У��Ҵ���Ũ����Ļ��Һû��Ѹ�ٴﵽ170��ȡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�������һ��������������������ϵ������������������˵������ȷ����(����)
A. 1 mol NaCl�����Ϊ22.4 L
B. 1 mol H2����6.02��1023�������
C. 1 mol O2����2 mol��ԭ��
D. ��״������1 mol H2�����Ϊ22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں������и����������Һ�У��ܴ�����������ҺΪ��ɫ�����ǣ���
A. Na+��Cu2+��Cl����SO42�D B. Ba2+��K+��OH����NO3�D
C. K+��Ca2+ ��NH4����CO32�D D. H+��Ca2+��Cl����HCO3�D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��������������Ϊ��Ҫ�Ķ�����Ԫ�أ��䵥�ʼ��������ڹ�ũҵ����������������Ҫ���á���ش��������⣺
��1�����ܱ�����������Ӧ���̱��������������ʹ1 mol N2��3 mol H2��Ϸ������з�Ӧ��N2(g)+3H2(g)![]() 2NH3(g) ��H=92.4 kJ��mol1������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ��֮����__________��������ƽ����ϵ���¶ȣ����������ƽ��ʽ��________���������С�����䡱�������ﵽƽ��ʱ�����������ڳ���1 mol N2��H2��ת����__________�����ߡ������͡����䡱�������ﵽƽ��ʱ����c(N2)��c(H2)��c(NH3)ͬʱ����1����ƽ��__________�ƶ������������������
2NH3(g) ��H=92.4 kJ��mol1������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ��֮����__________��������ƽ����ϵ���¶ȣ����������ƽ��ʽ��________���������С�����䡱�������ﵽƽ��ʱ�����������ڳ���1 mol N2��H2��ת����__________�����ߡ������͡����䡱�������ﵽƽ��ʱ����c(N2)��c(H2)��c(NH3)ͬʱ����1����ƽ��__________�ƶ������������������
��2�����������Ԫ���е�������ɵ�ij��ǿ�������εĻ�ѧʽΪ__________��������ˮ��________ˮ�ĵ��루��ٽ��������ơ�������ʹ��Һ��pH________������ߡ������͡����䡱����ԭ����____________________________�������ӷ���ʽ��ʾ����
��3�����������Ṥҵ��������Ҫԭ�ϣ��������������Ṥҵ�Ļ���������������ý������ֻ��������Ӧ������Ӧ����
4NH3(g)+5O2![]() 4NO(g)+6H2O(g) ��H=905 kJ��mol1 ��
4NO(g)+6H2O(g) ��H=905 kJ��mol1 ��
4NH3(g)+3O2(g)![]() 2N2(g)+6H2O(g) ��H=1268 kJ��mol1 ��
2N2(g)+6H2O(g) ��H=1268 kJ��mol1 ��
��������������Ӧ����NO���Ȼ�ѧ����ʽΪ__________________________��
��������¯�д�����ʱ���й����ʵIJ������¶ȵĹ�ϵ��ͼ������˵������ȷ����____________��

A����ҵ�ϰ�����������NOʱ������¶�Ӧ������780��840 ��֮��
B����ҵ�ϲ������ϱ�![]() ��1.7��2.0����Ҫ��Ϊ����߷�Ӧ����
��1.7��2.0����Ҫ��Ϊ����߷�Ӧ����
C����ѹ�����NH3����NO��ת����
D����ͼ��֪���¶ȸ���900 ��ʱ������N2�ĸ���Ӧ���࣬��NO���ʽ���
��4��M����Ҫ���л�����ԭ�ϣ��������H2O2������ͬ�ĵ���������1 mol M����������ȫȼ�գ�ֻ����1 mol CO2��2 mol H2O����M����ѧʽΪ__________��ij��ȼ�ϵ�ز��ò���Ϊ�缫��������KOH��ҺΪ����ʣ���MΪȼ�ϣ��Կ���Ϊ�����������õ�ع���ʱ����1 mol M�����·��ͨ��__________mol���ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����������������������ȷ���ǣ� ��
A. ��״���£�22.4LH2O���еķ�����ΪNA
B. ���³�ѹ�£�1.06g Na2CO3���е�Na+������Ϊ0.02 NA
C. ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4L
D. ���ʵ���Ũ��Ϊ0.5mol��L1��MgCl2��Һ�У�����Cl-����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Ļ�����A������Է�������Ϊ104��̼����������Ϊ92.3����
��1��A�ķ���ʽΪ__________________��
��2��A��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽΪ____________________________����Ӧ������________��
��3����֪��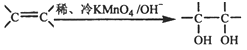 ����д��A��ϡ�����KMnO4��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ______________________________��
����д��A��ϡ�����KMnO4��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ______________________________��
��4��һ�������£�A��������Ӧ���õ��Ļ�������̼����������Ϊ85.7����д���˻�����Ľṹ��ʽ____________________________��
��5����һ�������£���A�ۺϵõ��ĸ߷��ӻ�����Ľṹ��ʽΪ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����÷�Ӧ2C+SiO2![]() Si+2CO��ұ���赥�ʣ��й�����������ǣ�������
Si+2CO��ұ���赥�ʣ��й�����������ǣ�������
A. ÿ��������������5.6gʱ������2.8g Si
B. �������ͻ�ԭ�������ʵ���֮��Ϊ1��2
C. �赥���ڳ����²����κ��ᡢ�Ӧ
D. ���ʹ��뵥��̼������һ���Ļ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊȷ���������ڿ����е������Ƿ���ʣ���ѡ�����Լ������������ʣ������ﵽĿ�ĵ���
A. KI��������Һ�� B. FeCl2��Һ��KSCN��
C. Na2SO3��Һ��BaCl2�� D. HCHO��Һ��ʯ����Һ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com