
| ʵ�鷽���벽�� | ʵ������ͽ��� |
| 1������������ͨ��ʢ������Ʒ����Һ���Թ��ڣ� | ��Ʒ����Һ��ɫ������ɫ��������SO2�� |
| 2��������ͨ��װ����������������Һ��ϴ��ƿ����С�Թ��ռ����壬���ھƾ����ϵ�ȼ | ���ռ����������ȼ�գ�����ɫ��������H2�� �������ʵ���֪������������ |
���� ��������衿��ʼ�������ȵ�Ũ���ᷴӦ�����ŷ�Ӧ�Ľ��У������Ϊϡ���ᣬ�����ڽ������˳����У���Ԫ��λ����Ԫ�ص�ǰ�ߣ���˿������е����û�����������Fe����ϡ���ᷴӦ�������������ݷ�Ӧ����������Ũ�ȴ�仯�����������ɿ��������¼������������һ����ɫ������SO2�����������ɫ������H2������������ɫ������SO2 ��H2 �Ļ�����壻
��ʵ����֤��1������������ͨ��ʢ������Ʒ����Һ���Թ��ڣ���Ʒ����Һ��ɫ��֤������SO2���壻
2��Ȼ������ͨ��װ����������������Һ��ϴ��ƿ��ȥ���к��е�SO2��������Ӧ��SO2+2NaOH=Na2SO3+H2O����С�Թ��ռ�ʣ�����壬���ھƾ����ϵ�ȼ�����۲쵽�������ȼ�գ�����Ϊ����ɫ����֤������H2��������ΪSO2 ��H2 �Ļ�����壮
��� �⣺��������衿���ŷ�Ӧ���У�Ũ������ϡ����˿��ϡ�����ܷ�Ӧ���������������ռ������������Ϊ��SO2��H2��SO2 ��H2 �Ļ�����壬��ͬѧԤ���������������ǣ����ŷ�Ӧ���У�Ũ�����ϡ����˿��ϡ�����ܷ�Ӧ�������������ݷ�Ӧ����������Ũ�ȴ�仯�����������ɿ��������¼������������һ����ɫ������SO2�����������ɫ������H2������������ɫ������SO2 ��H2 �Ļ�����壻
�ʴ�Ϊ�����ŷ�Ӧ���У�Ũ�����ϡ����˿��ϡ�����ܷ�Ӧ������������ɫ������H2��
��ʵ����֤��1����������������ʹƷ����Һ��ɫ�����Խ���������ͨ��ʢ������Ʒ����Һ���Թ��ڣ�Ʒ����Һ��ɫ��˵����ɫ��������SO2��
2��Ҫ��֤�����Ĵ��ڣ�Ҫ�ȳ�ȥ�����������壬Ȼ��ʣ��������ȼ�����������ȼ�գ�����ɫ��������H2��������ͨ��װ����������������Һ��ϴ��ƿ��ȥ���к��е�SO2��������Ӧ��SO2+2NaOH=Na2SO3+H2O����С�Թ��ռ�ʣ�����壬���ھƾ����ϵ�ȼ�����۲쵽�������ȼ�գ�����Ϊ����ɫ����֤������H2��������ΪSO2 ��H2 �Ļ������
�ʴ�Ϊ��
| ʵ�鷽���벽�� | Ԥ��ʵ������ͽ��� |
| Ʒ����Һ��ɫ | |
| ������ͨ��װ����������������Һ��ϴ��ƿ����С�Թ��ռ����壬���ھƾ����ϵ�ȼ�� | �ռ����������ȼ�� |
���� ������һ���ۺ������⣬�ȿ�����ѧ����֪ʶ����������ͬʱ�ֿ�����ѧ������ʵ��̽������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
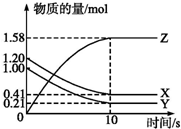 һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����κλ�ѧ��Ӧ��˵����Ӧ����Խ��Ӧ����Խ���� | |
| B�� | ��ѧ��Ӧ����Ϊ��0.8mol/��L•min������ʾ����˼�ǣ�ʱ��Ϊ1sʱ��ij���ʵ�Ũ��Ϊ0.8mol/L | |
| C�� | ��ѧ��Ӧ�ﵽƽ��״̬����Ӧֹͣ | |
| D�� | ��ѧ��Ӧ�����Ƕ���������ѧ��Ӧ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ø÷�Ӧ�����˹��̵� | |
| B�� | ��3mol N2��g����3mol H2��g����ϣ��ڸ��¡���ѹ�ʹ������³�ַ�Ӧ���ų�����92.22kJ | |
| C�� | ��Ϊ��Ӧ��Ҫ���ȣ����Է�Ӧ�ų����� | |
| D�� | ����������ͬʱ�����ø���Ч����������������߷�Ӧ���ʣ���������Ӧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H+��aq��+OH- ��aq��=H2O��l����H=-57.3 kJ•mol-1����֪��1 mol������������Һ�뺬0.5 mol�����ϡ��Һ��ϣ��ų���������57.3 kJ | |
| B�� | ��H2O��g��=H2O��l����H=-44.0kJ•mol-1��֪�Ƿ��ȷ�Ӧ�� | |
| C�� | ��SO2��g��+$\frac{1}{2}$O2��g��?SO3��g����H=-98.3 kJ•mol-1��֪�����ܱ������г���2 mol SO2��1 mol O2��ַ�Ӧ�ų�����Ϊ196.6 kJ | |
| D�� | ������ȼ���ȣ���H��Ϊ-285.5kJ/mo1����ˮ�����Ȼ�ѧ����ʽΪ��2H2O��1��=2H2��g��+O2��g����H=+285.5KJ/mo1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
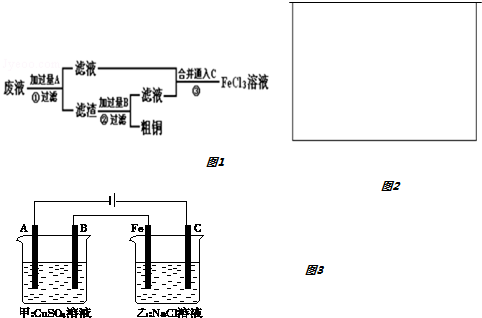
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������������������ֱ���ȫȼ�գ����߷ų������� | |
| B�� | �ɡ�C��ʯī���TC�����ʯ����H=1.9 kJ•mol����֪�����ʯ��ʯī�ȶ� | |
| C�� | ��101 kPaʱ��2 g H2 ��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H2O��l����H=-285.8 kJ/mol | |
| D�� | ��ϡ��Һ�У�H++OH-�TH2O��H=-57.3 kJ•mol��������1 mol H2SO4�뺬2 mol NaOH����Һ��ϣ��ų�����������114.6 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| �ܽ��� | �е� | �ܶȣ�g/mL�� | |
| �Ҵ� | ��ˮ���� | 78.5 | 0.8 |
| ������ | ������ˮ | 38.4 | 1.4 |
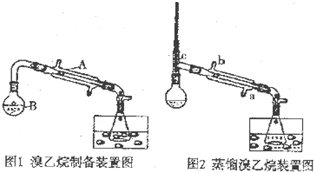
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʱ���������� pH ֵ��С | |
| B�� | ���ʱ��������Ӧ�ǣ�Ni��OH��2-2e-+2OH-=NiO2+2H2O | |
| C�� | �ŵ�ʱ�������Ϸ�����Ӧ��������Fe��OH��2 | |
| D�� | �ŵ�ʱ��������Ӧ�ǣ�NiO2+2e-+2H+=Ni��OH��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com