
判断正误,正确的划“√”,错误的划“×”
(1)海水提溴的过程中不发生氧化还原反应 ( )
(2)可以用淀粉溶液检验加碘食盐中的KIO3 ( )
(3)用CCl4萃取碘水中的碘,先振荡,后静置,液体分层,下层呈无色 ( )
(4)碘易升华,可用加热升华法除去NH4Cl中混有的I2 ( )
(5)能使湿润的淀粉KI试纸变蓝的气体一定是Cl2 ( )
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列关于SiO2和CO2的说法中正确的是 ( )
A.CO2、SiO2分别是碳酸和硅酸的酸酐
B.CO2和SiO2与水反应分别生成相应的酸
C.CO2是酸性氧化性,SiO2是两性氧化物
D.CO2和SiO2都是由相应的分子组成的
查看答案和解析>>
科目:高中化学 来源: 题型:
若两物质恰好完全反应,则下列各项中反应前后一定保持不变的是( )
①电子总数 ②原子总数 ③分子总数 ④物质的总能量 ⑤物质的总质量
A.①②⑤ B.①③⑤
C.②③④ D.②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
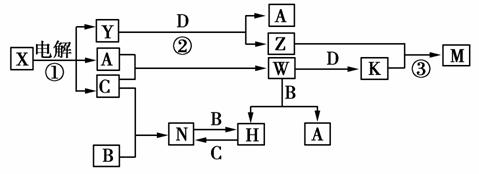
已知:A、B、C、D是单质,其余是化合物,其中B、D是常见金属,且组成B的元素属于过渡元素。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是__________________。
(2)写出N的化学式:________,并任写一种N的主要用途:_____
_________________________________________________________。
(3)写出下列反应的离子方程式:
反应①_______________________________________________。
反应③_______________________________________________。
K溶液和过量氨水反应_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.再通入少量氯气,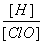 减小
减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有[Na+]=[Cl-]+[ClO-]
D.加入少量水,水的电离平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
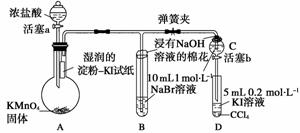
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是______________________________________。
(2)验证氯气的氧化性强于碘的实验现象是__________________________________。
(3)B中溶液发生反应的离子方程式是______________________________________。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_________________________
________________________________________________________________________。
(5)过程Ⅲ实验的目的是_______________________ ___________________________。
___________________________。
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下____________________,得电子能力逐渐减弱。
查看答案和解析>>
科目:高中化学 来源: 题型:
Br-形式存在于海水中,海水呈弱碱性。工业上制备Br2的操作步骤为
①一定条件下,将Cl2通入浓缩的海水中,生成Br2
②利用热空气将Br2吹出,并用浓Na2CO3溶液吸收,生 成NaBr、NaBrO
成NaBr、NaBrO 3等
3等
③用硫酸酸化步骤②得到的混合物
完成下列填空:
(1)Cl2氧化Br-应在__________条件下进行,目的是为了避免__________________。
(2)Br2可用热空气吹出,其原因是_________________________________________。
(3)写出步骤③所发生的化学反应方程式____________________________________。
用硫酸而不用盐酸酸化的原因可能是________________。步骤②的产品有时运输到目的地后再酸化,主要是因为___________________________________________________
________________________________________________________________________。
(4)为了除去工业Br2中微量的Cl2,可向工业Br2中___________________________。
a.通入HBr b.加入Na2CO3溶液
c.加入NaBr溶液 d.加入Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中Y所处的周期序数与主族序数之和为8。下列说法错误的是
A.Z元素的氧化物对应水化物的酸性一定弱于W
B.四种元素中Z的原子半径和形成的离子半径均最大
C.X、Z、W中最简单气态氢化物稳定性最弱的是Z
D.X、Y、Z的原子均能与氢原子形成四原子分子
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物丙由如下反应制得:
H2SO4(浓) Br2(CCl4)
C4H10O  C4H8
C4H8  C4H8Br2(丙),丙的结构简式不可能是
C4H8Br2(丙),丙的结构简式不可能是
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com