
| A. | 原子半径:X>Y>Z>Q>W | |
| B. | 最高价氧化物对应的水化物的酸性:Z<Q | |
| C. | Q和W可形成原子个数比为1:1和1:2的化合物 | |
| D. | X、Y和W三种元素形成的化合物的水溶液呈碱性 |
分析 Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,则X是Na元素;W、Z最外层电子数相同,二者位于同一主族,Z的核电荷数是W的2倍,则Z是S、W是O元素;工业上一般通过电解氧化物的方法获得Y的单质,则Y为Al元素;
五种元素核电荷数之和为54,Q原子序数=54-8-11-13-16=6,为C元素;
A.原子电子层数越多其原子半径越大,同一周期元素原子半径随着原子序数增大而减小;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
C.Q、W分别是C、O元素,二者可以形成CO和二氧化碳;
D.X、Y、W分别是Na、Al、O元素,形成的化合物是偏铝酸钠.
解答 解:Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色反应呈黄色,则X是Na元素;W、Z最外层电子数相同,二者位于同一主族,Z的核电荷数是W的2倍,则Z是S、W是O元素;工业上一般通过电解氧化物的方法获得Y的单质,则Y为Al元素;
五种元素核电荷数之和为54,Q原子序数=54-8-11-13-16=6,为C元素;
A.原子电子层数越多其原子半径越大,同一周期元素原子半径随着原子序数增大而减小,所以原子半径X>Y>Z>Q>W,故A正确;
B.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Z>Q,所以最高价氧化物对应的水化物的酸性:Z>Q,故B错误;
C.Q、W分别是C、O元素,二者可以形成CO和CO2,所以Q和W可形成原子个数比为1:1和1:2的化合物,故C正确;
D.X、Y、W分别是Na、Al、O元素,形成的化合物是偏铝酸钠,偏铝酸钠是强碱弱酸盐,其水溶液呈碱性,故D正确;
故选B.
点评 本题考查原子结构和元素周期律,侧重考查学生推断及元素周期律综合运用,明确原子结构、元素周期表结构、物质结构及物质性质是解本题关键,偏铝酸钠因为水解而导致其水溶液呈碱性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,相同体积的SO2和SO3,质量比为4:5 | |
| B. | 相同状况下,质量相同的O2和O3,密度之比为3:2 | |
| C. | 相同质量的金刚石和石墨含有相同的C原子数和共价键数 | |
| D. | 标准状况下,相同体积的C2H2和C2H4,密度比为13:14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4的水溶液导电性极弱:BaSO4?Ba2++SO42- | |
| B. | KHSO4在熔融状态下可导电:KHSO4=K++H++SO42+ | |
| C. | 常温下,0.1 mol/L的HF 溶液的pH>1:HF+H2O?H3O++F- | |
| D. | 向KI-淀粉溶液中滴加稀硫酸,溶液变蓝色:4I-+O2+2H2O=2I2+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v (NH3)=0.3 mol•L-1•min-1 | B. | v (H2)=0.3mol•L-1•min-1 | ||
| C. | v(N2)=0.2 mol•L-1•min-1 | D. | v (N2)=0.05mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和热测定实验用的小烧杯和物质的量浓度溶液配制用的容量瓶都必须干燥 | |
| B. | 用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液,若滴定终点时仰视读数,测得氢氧化钠浓度偏低 | |
| C. | 配制2.0 mol•L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确) | |
| D. | 用铜电极电解2.0 mol•L-1的硫酸,阴阳两极生成气体的体积之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
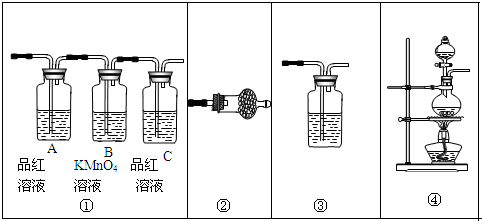
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com