
【题目】焰色反应实验过程中铂丝的清洗和灼烧与钾焰色反应的观察两项操作如图所示:
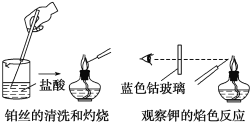
下列叙述中不正确的是
A.每次实验中都要先将铂丝灼烧到火焰无色,再蘸取被检验物质
B.钾的焰色反应要透过蓝色钴玻璃观察
C.实验时最好选择本身颜色较深的火焰
D.没有铂丝可用无锈铁丝代替进行实验
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】从元素化合价变化的角度分析,下列反应中,画线的物质发生氧化反应的是
A. SO2 + 2NaOH = Na2SO3 + H2O B. 2CuO + C![]() 2Cu + CO2↑
2Cu + CO2↑
C. 2FeCl3 + Fe = 3FeCl2 D. Zn+2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
A. 最终所得溶液中既有Fe2+又有Fe3+
B. 最终溶液中,硝酸无剩余
C. 标准状况下生成NO的体积为1.68 L
D. 再向最终所得溶液中滴加稀硝酸,无明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘酸钙[Ca(IO3)2]广泛用于食品工业、口腔洗涤,防腐等领域,某化学兴趣小组在实验室利用碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),溶液经氢氧化钾中和后,与氯化钙发生复分解反应制备碘酸钙,其制备步骤及装置(水浴加热装置略去)如图: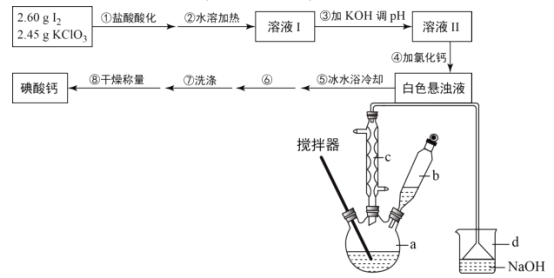
物质的摩尔质量如下表:
物质 | I2 | KClO3 | Ca(IO3)2 |
摩尔质量/g·mol-1 | 354 | 122.5 | 390 |
请回答下列问题:
(1)加入b中盐酸后,碘在酸性条件下被氯酸钾氧化成碘酸氢钾(KIO3·HIO3),反应中有黄绿色的气体生成,该反应的化学方程式为___。
(2)步骤②与“直接加热”相比,“水浴加热”的优点为___。
(3)步骤④加入氯化钙后,得到白色悬浊液,说明KIO3的溶解度___(填“大于”“小于”或“等于”)Ca(IO3)2。
(4)步骤⑤冰水浴冷却的目的为___。
(5)步骤⑥的操作名称为___。
(6)步骤⑦洗涤后检验沉淀是否洗涤干净的方法为___。
(7)最终得到2..60g碘酸钙产品,则产率为___ %(保留2小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标出下列反应电子转移的方向和总数:
2Fe(NO3)3 + 16NaOH + 3Cl2 → 2Na2FeO4 + 6NaNO3 + 6NaCl + 8H2O________________
(1)反应中______元素被氧化, 还原剂是__________, 还原产物是_______,发生还原反应的物质是_________
(2)若反应中转移了0.2 mol电子,则消耗了_______L Cl2(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸(![]() ) 是乳酸菌在肠道通过代谢产生,是近年来研究的热点。
) 是乳酸菌在肠道通过代谢产生,是近年来研究的热点。
(1)乳酸可发生的化学反应类型有__________。
a.取代反应 b.加成反应 c.氧化反应 d.还原反应
(2)与乳酸含有相同官能团的同分异构体的结构简式_______________。
(3)相同物质的量的乳酸分别与足量的金属钠和氢氧化钠溶液反应,消耗的金属钠与氢氧化钠的物质的量之比是__________。
(4)两个乳酸分子在一定条件下发生酯化反应既能生成六元环状化合物M,又能得到链状化合物N,则M、N的结构简式分别是________,________。
(5)可降解一次性餐盒是由乳酸在一定条件下通过___________(填反应类型)生成的高分子材料制得,合成这种高分子材料的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的反应判断下列说法中错误的是
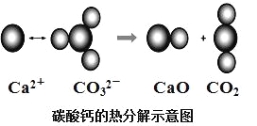
A. CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量
B. 该反应的焓变大于零
C. 该反应中有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量
D. 由该反应可推出凡是需要加热才发生的反应均为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硝酸铵的流程如下图所示:
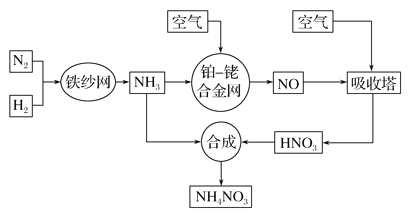
请回答下列问题:
(1)已知:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ· mol-1。
2NH3(g) ΔH=-92.4 kJ· mol-1。
①在500 ℃、2.02×107 Pa和铁催化条件下向一密闭容器中充入1 mol N2和3 mol H2,充分反应后,放出的热量________(填“大于”、“小于”或“等于”)92.4 kJ。
②为提高H2的转化率,实际生产中宜采取的措施有________(填字母)。
A.降低温度
B.最适合催化剂活性的适当高温
C.适当增大压强
D.减小压强
E.循环利用和不断补充氮气
F.及时移出氨
(2)该流程中铂—铑合金网上的氧化还原反应为4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。
4NO(g)+6H2O(g)。
①已知铂—铑合金网未预热也会发热,则随着温度升高,该反应的化学平衡常数K________(填“增大”、“减小”或“不变”),理由是__________________________________________________________________。
②若其他条件不变,则下列图像正确的是________(填字母)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上研究高效处理煤燃烧释放出来的SO2,有利于减小环境污染。在T℃时,利用CO处理SO2的反应为:2CO(g)+SO2(g)![]() 2CO2(g)+S(l) △H=akJ/mol;
2CO2(g)+S(l) △H=akJ/mol;
(1)已知T℃时:C(s)+![]() O2(g)=CO(g) △H1=-110.5kJ/mol
O2(g)=CO(g) △H1=-110.5kJ/mol
S(l)+O2(g)=SO2(g) △H2=-290.0kJ/mol
C(s)+O2(g)=CO2(g) △H3=-390.0kJ/mol
则T℃时,a=___。
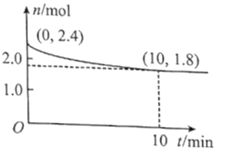
(2)在T℃下,将1.4molCO和1molSO2通入2L恒容容器中发生上述反应,反应体系气体总物质的量随时间变化如图;在0~10min,反应的平均速率v(CO)=___,SO2的平衡转化率![]() (SO2)=___%;在T℃时该反应的平衡常数Kc=___L/mol。
(SO2)=___%;在T℃时该反应的平衡常数Kc=___L/mol。
(3)实验测得:v正=v(CO)消耗=k正c(CO)c(SO2),v逆=v(CO2)消耗=k逆![]() ,k正、k逆为只受温度影响的速率常数。若将(2)中容器内的温度升高(假设各物质的状态不发生变化),
,k正、k逆为只受温度影响的速率常数。若将(2)中容器内的温度升高(假设各物质的状态不发生变化),![]() 的值将___(填“增大”、“减小”或“不变”)。
的值将___(填“增大”、“减小”或“不变”)。
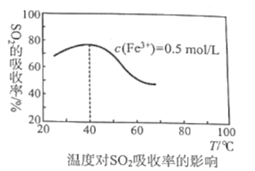
(4)某科研团队研究用Fe2(SO4)3(aq)处理SO2:Fe3+溶液吸收SO2发生的离子反应方程式为___;其他外界条件不变下,在相同时间内温度对SO2吸收率的影响结果如图,在40℃前,SO2的吸收率随温度变化的可能原因是___;在40℃后,SO2的吸收率发生的变化是温度升高该反应逆向移动的结果,导致反应逆向移动的原因:一是该反应为放热反应,二是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com