
(10·Ö) ²āµĆij½šŹōŅ±Į¶³§µÄĖįŠŌ¹¤Ņµ·ĻĖ®ÖŠ£¬ŗ¬ÓŠŅ»¶ØĮæµÄFe3+”¢Cu2+”¢Au3+µČĄė×Ó”£°“ÕÕ”°±ä·ĻĪŖ±¦”±µÄŌŌņ£¬Éč¼ĘĮĖĻĀĶ¼ÖŠµÄ»ŲŹÕĮ÷³Ģ£¬ŅŖĒóĄūÓĆ³£¼ūµÄĖį”¢¼īŗĶ¹¤ŅµÉś²śÖŠµÄ·ĻĢśŠ¼£¬“ÓøĆ¹¤Ņµ·ĻĖ®ÖŠ»ŲŹÕ½š”¢²¢Éś²ś»Æ¹¤ŌĮĻĢśŗģŗĶŃõ»ÆĶ”£

ĒėÄćĶź³ÉĻĀĆęµÄĪŹĢā£ŗ
£Ø1£©Į÷³ĢĶ¼ÖŠ±źŗÅ“¦Šč¼ÓČėµÄĻąÓ¦ĪļÖŹ·Ö±šŹĒ£ŗ¢Ł £»¢Ś £»
¢Ū £»¢Ü £»¢Ż ”£
£Ø2£©Š“³öĮ÷³ĢĶ¼ÖŠ¢Ł“¦æÉÄÜ·¢ÉśµÄĖłÓŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
£Ø3£©Š“³öĮ÷³ĢĶ¼ÖŠ¢Ū“¦·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø1£©¢ŁĢśŠ¼ ¢ŚĻ”ĮņĖį ¢ŪĻ”ĻõĖį ¢ÜĒāŃõ»ÆÄĘ ¢ŻĒāŃõ»ÆÄĘ
£Ø2£© Fe+2H+==Fe2++ H2”ü£»2Fe3++Fe==3Fe2+£»Cu2++Fe=Cu+Fe2+£»2Au3++3Fe=2Au + 3Fe2+
£Ø3£© 3Cu+8HNO3(Ļ”)==3Cu(NO3)2Ź®2NO”üŹ®+4H2O
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗĻņ¹¤Ņµ·ĻĖ®ÖŠŹ×ĻČ¼ÓČė×ćĮæµÄFeŠ¼£¬·¢ÉśÖĆ»»·“Ó¦£¬µĆµ½µÄ¹ĢĢåAÖŠŗ¬ÓŠ²śÉśAu”¢Cuµ„ÖŹ¼°¹żĮæµÄFe,ŌŚĀĖŅŗEÖŠŗ¬ÓŠFe2+£»ĻņĀĖŌüÖŠ¼ÓČėĻ”ĮņĖįČܽā¹żĮæµÄFe£¬°ŃĀĖŅŗÓėEŗĻ²¢£¬ŌŁĻņĘäÖŠ¼ÓČė¹żĮæµÄNaOHČÜŅŗ,×īÖÕµĆµ½³ĮµķF£ŗFe(OH)3£¬½«³Įµķ¹żĀĖ³öĄ“£¬Ļ“µÓøɾ»²¢×ĘÉÕ£¬µĆµ½ĢśŗģFe2O3£»Ļņŗ¬ÓŠŗ¬ÓŠAu”¢CuµÄĀĖŌüBÖŠ¼ÓČėĻ”ĻõĖį£¬Cu·¢Éś·“Ó¦²śÉśCu(NO3)2£»Au²»·¢Éś·“Ó¦£¬¹żĀĖ³öĄ“£¬ĻņĀĖŅŗCÖŠ¼ÓČė×ćĮæµÄĒāŃõ»ÆÄĘČÜŅŗ£¬²śÉśCu(OH)2³Įµķ£¬½«³Įµķ¹żĀĖ³öĄ“£¬Ļ“µÓøɾ»²¢×ĘÉÕ£¬µĆµ½ĢśŗģCuO”££Ø1£©Į÷³ĢĶ¼ÖŠ±źŗÅ“¦Šč¼ÓČėµÄĻąÓ¦ĪļÖŹ·Ö±šŹĒ£ŗ¢ŁĢśŠ¼£¬ ¢ŚĻ”ĮņĖį£¬¢ŪĻ”ĻõĖį£¬¢ÜĒāŃõ»ÆÄĘ£¬¢ŻĒāŃõ»ÆÄĘ£»£Ø2£©ŌŚĮ÷³ĢĶ¼ÖŠ¢Ł“¦æÉÄÜ·¢ÉśµÄĖłÓŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒFe+2H+==Fe2++ H2”ü£»2Fe3++Fe==3Fe2+£»Cu2++Fe=Cu+Fe2+£»2Au3++3Fe=2Au + 3Fe2+£» £Ø3£©ŌŚĮ÷³ĢĶ¼ÖŠ¢Ū“¦·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ3Cu+8HNO3(Ļ”)= 3Cu(NO3)2Ź®2NO”üŹ®+4H2O”£
æ¼µć£ŗ漲鹤Ņµ·ĻĖ®µÄ×ŪŗĻĄūÓĆµÄ¹ż³Ģ”¢ŌĄķ”¢·½³ĢŹ½µÄŹéŠ“µÄÖŖŹ¶”£


 ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģŗÓ±±Ź”ŹÆ¼Ņ×ÆŹŠĪ劣ĮŖæ¼øßČżÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÖŠ²»ÕżČ·µÄŹĒ
A£®·ÖŅŗŹ±£¬·ÖŅŗĀ©¶·ÖŠĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬ÉĻ²ćŅŗĢå“ÓÉĻæŚµ¹³ö
B£®ÕōĮóŹ±£¬Ó¦Ź¹ĪĀ¶Č¼ĘĖ®ŅųĒņææ½üÕōĮóÉÕĘæÖ§¹ÜæŚ“¦
C£®µĪ¶ØŹ±£¬×óŹÖæŲÖʵĪ¶Ø¹Ü»īČū£¬ÓŅŹÖĪÕ³Ö׶ŠĪĘ棬±ßµĪ±ßÕńµ“£¬ŃŪ¾¦×¢ŹÓµĪ¶Ø¹ÜÖŠµÄŅŗĆę
D£®ÅäÖĘĀČ»ÆĢśČÜŅŗŹ±£¬½«Ņ»¶ØĮæĀČ»ÆĢśČܽāŌŚ½ĻÅصÄŃĪĖįÖŠ£¬ŌŁÓĆĖ®Ļ”ŹĶµ½ĖłŠčÅضČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”ŗģÉ«ĮłŠ£øßČżµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éÓŠ»śĪļÖ»ÓĆŅ»ÖÖŹŌ¼ĮĪŽ·Ø¼ų±šµÄŹĒ£Ø £©
A£®ŅŅ“¼”¢¼×±½”¢Ļõ»ł±½ B£®±½”¢¼×±½”¢»·¼ŗĶé
C£®±½”¢±½·Ó”¢¼ŗĻ© D£®¼×Ėį”¢ŅŅČ©”¢ŅŅĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”ÉĻѧʌøßČżµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ×°ÖĆÓ¦ÓĆÓŚŹµŃéŹŅÖĘĀČĘų²¢»ŲŹÕĀČ»ÆĆĢµÄŹµŃ飬ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ£Ø £©
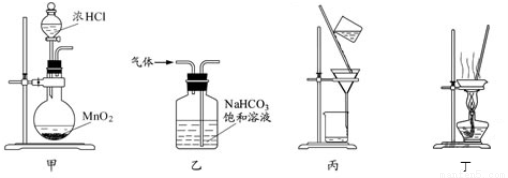
A£®ÓĆ×°ÖĆ¼×ÖĘČ”ĀČĘų B£®ÓĆ×°ÖĆŅŅ³żČ„ĀČĘųÖŠµÄÉŁĮæĀČ»ÆĒā
C£®ÓĆ×°ÖƱū·ÖĄė¶žŃõ»ÆĆĢŗĶĀČ»ÆĆĢČÜŅŗ D£®ÓĆ×°Öƶ”ÕōøÉĀČ»ÆĆĢČÜŅŗÖĘMnCl2?4H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”ÉĻѧʌøßČżµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
(NAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ) ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®25”ꏱ£¬pH=13µÄ1.0L Ba(OH) 2ČÜŅŗÖŠŗ¬ÓŠµÄ ŹżÄæĪŖ0£®2NA
ŹżÄæĪŖ0£®2NA
B£®±ź×¼×“æöĻĀ£¬11.2LµÄĪģĶéĖłŗ¬µÄ·Ö×ÓŹżĪŖ0.5NA
C£®±ź×¼×“æöĻĀ£¬2.24 L Cl2ČÜÓŚĖ®ÖŠ“ļµ½±„ŗĶ£¬×ŖŅʵĵē×ÓŹżŹĒ0.1NA
D£®ĻÖÓŠŅŅĻ©”¢±ūĻ©”¢¶”Ļ©µÄ»ģŗĻĘųĢå¹²14g£¬ĘäŌ×ÓŹżĪŖ3NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”øßČżµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijæĪĶā»ī¶ÆŠ”×éµÄĶ¬Ń§Óū²ā¶Ø¹żŃõ»ÆÄĘÓėĢ¼ĖįÄĘ»ģŗĻĪļÖŠ¹żŃõ»ÆÄʵÄÖŹĮæ·ÖŹż£¬ĖūĆĒĻČ×¼Č·³ĘĮæĮĖaæĖѳʷ£¬ĒėÄćÅŠ¶Ļ£¬ŌŚŅŌĻĀÉč¼ĘµÄø÷²½ŗóŠųŹµŃé·½°øÖŠ£¬²»ŗĻĄķµÄŹĒ
A£®øō¾ųæÕĘų¼ÓČČ£¬ĄäČ“ŗ󣬳ĘĮæŹ£Óą¹ĢĢåÖŹĮæĪŖm 1 g
B£®Óė×ćĮæĻ”ŃĪĖį·“Ó¦²¢ÕōøÉ£¬³ĘĮæŹ£Óą¹ĢĢåÖŹĮæĪŖm 2 g
C£®Óė×ćĮæĖ®·“Ó¦²¢¼ÓČČ£¬ŹÕ¼Æµ½±ź×¼×“æöĻĀV1 LøÉŌļĘųĢå
D£®Óė×ćĮæĻ”ĮņĖį·“Ó¦²¢¼ÓČČ£¬ŹÕ¼Æµ½±ź×¼×“æöĻĀV2 L øÉŌļĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”øßČżµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓŠ¹ŲĪļÖŹµÄŠŌÖŹŗĶøĆŠŌÖŹµÄÓ¦ÓĆ¾łÕżČ·µÄŹĒ
A£®¾§Ģå¹č¾ßÓŠ°ėµ¼ĢåŠŌÖŹ£¬æÉÓĆÓŚÉś²ś¹āµ¼ĻĖĪ¬
B£®H2O2ŹĒŅ»ÖÖĀĢÉ«Ńõ»Æ¼Į£¬æÉÓėĖįŠŌøßĆĢĖį¼Ų×÷ÓĆ²śÉśO2
C£®ĶµÄ½šŹō»ī¶ÆŠŌ±ČĢśČõ£¬æÉÓĆĶ¹Ž“śĢęĢś¹ŽÖü“ęŗĶŌĖŹäÅØĮņĖį»ņÅØĻõĖį
D£®ĀĮ¾ßÓŠĮ¼ŗƵĵ¼µēŠŌ£¬øÖæ¹ĄĒæ¶Č“ó£¬øÖŠ¾ĀĮ½ŹĻßæÉÓĆ×÷Ō¶¾ąĄėøßŃ¹ŹäµēĻß²ÄĮĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”ŠĀÓąŹŠøßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŹµŃéµÄŠšŹö£¬ÕżČ·µÄŹĒ
A£®ÓĆ¹ć·ŗpHŹŌÖ½²āµĆĀČĖ®µÄpHĪŖ2
B£®ÓĆĶŠÅĢĢģĘ½³ĘČ”10.50gøÉŌļµÄNaCl¹ĢĢå
C£®ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄČÜŅŗ£¬¶ØČŻŹ±ø©ŹÓČŻĮæĘæµÄæĢ¶ČĻߣ¬»įŹ¹ĖłÅäČÜŅŗµÄÅضČĘ«øß
D£®ÖʱøFe(OH )2Ź±£¬ĻņFeSO4ČÜŅŗÖŠµĪČėNaOHČÜŅŗŹ±£¬½ŗĶ·µĪ¹Ü²»ÄÜÉģČėŅŗĆęŅŌĻĀ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ½Ī÷Ź”øßČżÉĻѧʌµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÄÜÕżČ·±ķŹ¾ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ
A£®Fe3O4ČÜÓŚ×ćĮæĻ”HNO3£ŗFe3O4£«8H£«=Fe2£«£«2Fe3£«£«4H2O
B£®µČĪļÖŹµÄĮæµÄMgCl2”¢Ba(OH)2 ŗĶ HC1 ČÜŅŗ»ģŗĻ£ŗMg2£«£«2OH£= Mg(OH)2”ż
C£®½«¹żĮæµÄSO2ĶØČėCa(ClO)2ČÜŅŗÖŠ£ŗ SO2+ClO£+H2O =HClO+ HSO3-
D£®½«0.2 mol”¤L£1µÄNH4Al(SO4)2ČÜŅŗÓė0.3 mol”¤L£1µÄBa(OH)2ČÜŅŗµČĢå»ż»ģŗĻ£ŗ
2Al3£«£«3SO £«3Ba2£«£«6OH£=2Al(OH)3”ż£«3BaSO4”ż
£«3Ba2£«£«6OH£=2Al(OH)3”ż£«3BaSO4”ż
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com