
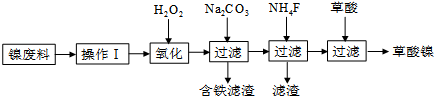
分析 流程分析,镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4•2H2O),再高温煅烧草酸镍制取三氧化二镍.镍废料加入酸溶解后过滤得到滤液中含有亚铁离子、钙离子、镁离子、镍离子,加入过氧化氢氧化亚铁离子为铁离子,加入碳酸钠溶液调节溶液的PH,使铁离子全部沉淀,过滤后的滤液在加入NH4F沉淀钙离子和镁离子,过滤得到溶液含有捏离子的溶液,在溶液中加入草酸生成草酸镍,蒸发浓缩结晶析出晶体为目标产物NiC2O4•2H2O,
(1)镍废料中主要是镍、铁、钙、镁合金为主,操作Ⅰ是酸溶后过滤,溶解金属,除去不溶物;
(2)过氧化氢氧化亚铁离子为铁离子,依据电荷守恒和原子守恒,加入Na2CO3溶液调pH至4.0〜4.5,促进铁离子水解形成氢氧化铁沉淀;
(3)草酸镍(NiC2O4•2H2O)在热空气中干燥脱水后生成NiC2O4,NiC2O4再发生氧化还原反应(Ni由+2价升高到+3价,则C由+3价降低到+2价,题中要求生成混合气体,则另一气体为CO2)生成Ni2O3、CO、CO2,再利用化合价升降相等配平;
(4)Cl由+1价降低到-1价,Ni由+2价升高到+3价,利用化合价升降相等可配平ClO-、Ni(OH)2、Cl-、Ni2O3的系数,再利用H原子守恒配平水的系数,最后可利用O原子检查配平是否正确;依据化学方程式和元素守恒计算得到;
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,发生还原反应,则Al发生氧化反应,碱性条件下得到NaAlO2,配平书写方程式.
解答 解:(1)分析框图:“酸溶”生成含镍、铁、钙、镁离子的溶液,加酸溶解,溶解金属,除去不溶物过滤;
故答案为:加酸溶解,过滤;
(2)加双氧水的目的是氧化生成Fe3+,反应的离子方程式为:2Fe2++H2O2+2H+═2Fe3++2H2O,加入碳酸钠溶液的作用是调节pH,促进铁离子水解沉淀完全,;
故答案为:2Fe2++H2O2+2H+═2Fe3++2H2O,促进铁离子水解沉淀完全;
(3)草酸镍(NiC2O4•2H2O)在热空气中干燥脱水后生成NiC2O4,NiC2O4再发生氧化还原反应(Ni由+2价升高到+3价,则C由+3价降低到+2价,题中要求生成混合气体,则另一气体为CO2)生成Ni2O3、CO、CO2,再利用化合价升降相等,Ni:升高2×(3-2),C:升高1×(4-3),C:降低:3×(3-2),配平方程式为:2NiC2O4$\frac{\underline{\;高温\;}}{\;}$Ni2O3+3CO↑+CO2↑;
故答案为:2NiC2O4$\frac{\underline{\;高温\;}}{\;}$Ni2O3+3CO↑+CO2↑;
(4)Cl由+1价降低到-1价,Ni由+2价升高到+3价,利用化合价升降相等可配平ClO-、Ni(OH)2、Cl-、Ni2O3的系数,再利用H原子守恒配平水的系数,最后可利用O原子检查配平是否正确,得到离子方程式为:ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O;
ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O
1 2
n(ClO-) a mol
则n(ClO-)=0.5 a mol
Cl2+2OH-═ClO-+Cl-+H2O
0.8n(Cl2) 0.5 a mol
则n(Cl2)=0.625 a mol
进行电解时:
2Cl--2e-═Cl2↑
2 1
n(e-) 0.625 a mol
则n(e-)=1.25a mol;
故答案:ClO-+2Ni(OH)2═Cl-+Ni2O3+2H2O;1.25a mol;
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,发生还原反应,则Al发生氧化反应,碱性条件下得到NaAlO2,该电池反应的化学方程式是:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2,
故答案为:Al+3NiO(OH)+NaOH+H2O=3Ni(OH)2+NaAlO2.
点评 本题考查了流程分析推断,实验操作步骤的分析判断,化学方程式计算和电解原理分析应用,题目综合性较大,难度较大.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
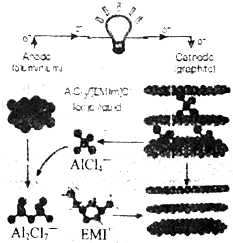 2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )
2015年4月,由中美科学家共同完成的“快速充放电铝离子电池”,具有高效耐用、可超快充电、可燃性低、成本低等特点.该电池以金属铝作为负极,三维结构的泡沫石墨材料为正极,AlCl4-可在其中或在脱嵌,由有机离子 (EMI+不参与反应)Al2Cl7-和AlCl4-组成的离子液体做电解质溶液,该电池放电时的原理如图所示,下列说法正确的是( )| A. | 放电时,负极的电极反应式:Al-3e-+7AlCl4-═Al2C17- | |
| B. | 充电过程中,AlCl4-脱嵌并从阴极向阳极迁移 | |
| C. | 充电过程中阳极的电极反应式为:Cn+AlCl4--e-═Cn,其中C的化合价升高 | |
| D. | 该离子液体也可用于钢制品上电镀铝,但阴极材料要换成镀件 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
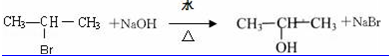 ;
;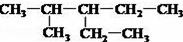 ;
;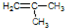 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO>HBrO4>HIO4 | B. | 碱性:Al(OH)3>Mg(OH)2>NaOH | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 非金属性:F>O>S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,分子数为NA的CO和C2H4混合气体的质量为28g | |
| B. | 标准状况下,20g重水(D2O)中含有的中子数为10NA | |
| C. | 用MnO2与浓盐酸制取Cl2时,每生成0.5mol Cl2则转移电子数为NA | |
| D. | 0.1 L 3.0 mol•L-1的NH4NO3溶液中含有NH4+的数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、油脂都属于高分子化合物 | |
| B. | 能发生酯化反应的酸不一定都是羧酸 | |
| C. | 天然蛋白蛋水解的最终产物是一种氨基酸,这种氨基酸有两性 | |
| D. | 油脂水解得到的醇是丙三醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑦ | B. | ⑤⑦ | C. | ③⑤ | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ④⑤⑥ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com