
���� ��1��������������ʲ��ֵ��룻
��2����25��ʱ��KW=C��H+����C��OH-��=10-14��C��OH-��=$\frac{{K}_{w}}{c��{H}^{+}��}$��PH=-lgC��H+��������AG��pH�ļ��㹫ʽ�ɵ�AG=lg$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=lg$\frac{c��{H}^{+}��}{\frac{1{0}^{-14}}{c��{H}^{+}��}}$=2��7-pH��������pH=3�Ĵ�����Һ��AG=2��7-3��=8��
��3���ٴ���Ϊ���ᣬ����Ϊǿ�ᣬ��Ũ��ʱ�����pH��
�ڴ�������ʾ���ԣ��Ȼ�����ʾ���ԣ�
��0.1mol•L-1 NaOH��Һ10mL����Һ���Ϊ20.00mL0.1mol•L-1�Ĵ��ᷴӦ���õ����Ǵ���ʹ����ƵĻ����ݴ�ȷ������Ũ�ȴ�С��
��� �⣺��1��������������ʲ��ֵ��룬���뷽��ʽΪ��CH3COOH?CH3COO-+H+���ʴ�Ϊ��CH3COOH?CH3COO-+H+��
��2����25��ʱ��KW=C��H+����C��OH-��=10-14��C��OH-��=$\frac{{K}_{w}}{c��{H}^{+}��}$��PH=-lgC��H+��������AG��pH�ļ��㹫ʽ�ɵ�AG=lg$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=lg$\frac{c��{H}^{+}��}{\frac{1{0}^{-14}}{c��{H}^{+}��}}$=2��7-pH��������pH=3�Ĵ�����Һ��AG=2��7-3��=8���ʴ�Ϊ��8��
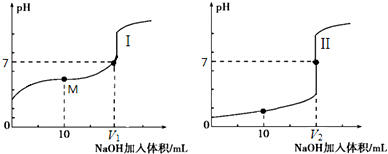
��3������ͼ��δ��NaOHʱ��pH��֪��ͼ�������pH����1��ͼ�������pH=1��˵����Ϊ0.1mol/L��������Һ��Ϊ������Һ�ζ����̣����Եζ������������I��
�ʴ�Ϊ��I��
�ڴ������������֮��ķ�Ӧ����ǡ����ȫ��Ӧ�õ��Ĵ�������ʾ���ԣ�Ҫʹ����Һ��ʾ���ԣ�pH=7����Ҫ�����Թ����������������������ǡ����ȫ��Ӧ���õ����Ȼ�����ʾ���ԣ�����V1��V2���ʴ�Ϊ������
����0.1mol•L-1 NaOH��Һ10mL����Һ���Ϊ20.00mL0.1mol•L-1�Ĵ��ᷴӦ���õ����Ǵ���ʹ����ƵĻ�����ʾ���ԣ���ʱ����Ũ�ȴ�Сc��CH3COO-����c ��Na+����c ��H+����c ��OH-�����ʴ�Ϊ��c��CH3COO-����c ��Na+����c ��H+����c ��OH-����
���� �����ۺϿ���ѧ�����ζ��Լ���Һ������Ũ�ȴ�С�Ƚϵ�֪ʶ�������ۺ�֪ʶ�Ŀ��飬ͼ������ж��ǽ���ؼ������ջ����ǹؼ����ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������6 mol•L-1������ | B�� | ������������ˮ | ||
| C�� | ���� | D�� | ��п�����пƬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| �������� | ZnƬ��ʯī | ZnƬ��CuƬ | CuƬ��AgƬ | FeƬ��CuƬ |
| ������Һ | CuSO4��Һ | ��ˮ�ƾ� | AgNO3��Һ | ϡ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �Թ� | ���� | ���� |
| a | ���Թ��м���NaBr��Һ���μ�������ˮ���������ټ�������CCl4������ | CCl4������ɫ��Ϊ�Ⱥ�ɫ |
| b | �������Թ��м���FeCl2��Һ���μ�����KSCN��Һ ��������������ˮ���� | ����dz��ɫ��Һ�����Ա仯 ������Һ��Ϊ��ɫ |
| ���� | A������ |
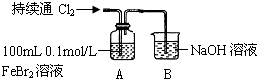 | ������ʼͨ��100mL���ۺϱ�״����Cl2����Һ��dz��ɫ��� ��������ͨ��Cl2����Һ��ɫ�������Ϊ�ػ�ɫ��ֹͣͨ��Cl2 |
| �Թ� | ���� | ���� |
| c | �μ�2-3��KSCN��Һ���� | ��Һ��ΪѪ��ɫ |
| d | ��������CCl4�������� | ���ֲַ������²�Ϊ���Ȼ�̼���ҳ���ɫ |
| �Թ� | ���� | ���� |
| e | ���Թ��м���2mL�ػ�ɫ��Һ����������CCl4�������� | CCl4������ɫ��Ϊ�Ⱥ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ǿ����H2SiO3��H2CO3��H2SO4 | B�� | ���ȶ��ԣ�HCl��HBr��HI | ||
| C�� | ԭ�Ӱ뾶��Na��Mg��Al | D�� | �۵㣺SiO2��NaCl��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������۵�ܵͣ����������������²��� | |
| B�� | �⻯ѧ����������ŷ�̼�⻯����͵����������й� | |
| C�� | ��ˮ�Ҵ�����ҽ��������Ч������ | |
| D�� | Na��S��C�ֱ��������е�ȼ���ɵõ����ֲ�ͬ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com