
下列关于物质或离子检验的叙述正确的是
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.某溶液中加入稀硫酸,放出无色无味气体,将该气体通入澄清石灰水,溶液变浑浊,证明原溶液中一定含有CO32-
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源:2015-2016学年江西省高一上第三次考试化学试卷(解析版) 题型:实验题
某学生为了探究钠与CO2的反应,利用如图装置进行实验.(已知PdCl2能被CO还原得到黑色的Pd)
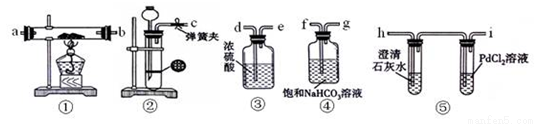
(1)请将上图各装置连接完整(填写装置中字母):c接f, 接 , 接 ,接 。
(2)若用稀盐酸与CaCO3反应制备CO2,在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是 。
A.NaNO3溶液 B.CCl4 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到 时再点燃酒精灯。
(4)反应过程中CO2足量,假如反应过程中有下列两种情况,分别写出两种情况下钠与CO2反应的化学方程式 。
Ⅰ.装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体 。
Ⅱ.装置①中钠的质量为0.46g,充分反应后,将装置①中的固体加入到足量稀盐酸中产生224mL(标准状况)CO2气体,且溶液中还有固体残留 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一上期中测试化学试卷(解析版) 题型:选择题
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
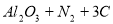

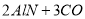
下列有关该反应的叙述正确的是
A、氮化铝中氮元素的化合价为-3
B、上述反应中每生成2molAlN,N2得到3mol电子
C、在氮化铝的合成反应中,N2是氧化剂,Al2O3是还原剂
D、该反应不属于四种基本反应类型中任一种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏六盘山中学高二上第二次月考化学试卷(解析版) 题型:选择题
25 ℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上11月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.与28gCO具有相同分子数的CO2的质量一定是44 g
B.与V LCO具有相同分子数的CO2的体积一定是V L
C.所含原子数相等的CO与CO2的密度之比为7∶11
D.所含原子数相等的CO与CO2的密度之比为21∶22
查看答案和解析>>
科目:高中化学 来源:2016届贵州市高三上学期第四次月考理综化学试卷(解析版) 题型:推断题
A、B、C、D、E、F六种短周期主族元素,其原子序数依次增大,其中B与C同周期,D与E和F周周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D所在周期原子半径最大的主族元素,又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素F在周期表中的位置_______________________;
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)____________;
(3)由A、B、C三种元素以原子个数比4:2:3形成化合物X,X中所含化学键类型有_________;检验该化合物中的阳离子的方法是____________________(用离子方程式表示及文字描述表示)。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出D元素的最高价氧化物对应的水化物与E的最高价氧化物反应的离子方程式:_______________________;若E是非金属元素,其单质在电子工业中有重要应用,请写出其单质溶于强碱溶液的离子方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期12月模拟化学试卷(解析版) 题型:选择题
下列有关实验操作设计、现象记录、结论解释都正确的是
实验操作设计 | 现象记录 | 结论解释 | |
A | 用坩埚钳夹住铝箔在酒精灯 上加热 | 铝箔熔化但并不滴落 | 熔点:Al2 O3>Al |
B | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
C | 向某氯化亚铁溶液中加入 Na2O2粉末 | 出现红褐色沉淀 | 加入Na2O2粉末前,原氯化 亚铁溶液已经变质 |
D | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中含有Na+,无K+ |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北邯郸魏县一中、曲周县一中高二上期中化学试卷(解析版) 题型:填空题
质子交换膜燃料电池广受关注.
(1)质子交换膜燃料电池中作为燃料的H2通常来自水煤气.
已知:C(s)+1/2O2(g)═CO(g) △H1=﹣110.35kJ·mol﹣1
2H2O(l)═2H2(g)+O2(g) △H2=+571.6kJ·mol﹣1
H2O(l)═H2O(g) △H3=+44.0kJ·mol﹣1
则C(s)+H2O(g)═CO(g)+H2(g) △H4= .
(2)燃料气(流速为1800mL·h﹣1;体积分数为50% H2,0.98% CO,1.64% O2,47.38% N2)中的CO会使电极催化剂中毒,使用CuO/CeO2催化剂可使CO优先氧化而脱除.
①160℃、CuO/CeO2作催化剂时,CO优先氧化反应的化学方程式为 .
②灼烧草酸铈[Ce2(C2O4)3]制得CeO2的化学方程式为 .
③在CuO/CeO2催化剂中加入不同的酸(HIO3或H3PO4),测得燃料气中CO优先氧化的转化率随温度变化如图1所示.加入 (填酸的化学式)的CuO/CeO2催化剂催化性能最好.催化剂为 - HIO3,120℃时,反应1h后CO的体积为 mL.
- HIO3,120℃时,反应1h后CO的体积为 mL.

(3)图2为甲酸质子交换膜燃料电池的结构示意图.该装置中 (填“a”或“b”)为电池的负极,负极的电极反应式为
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省盐城市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列有关使用托盘天平的叙述,不正确的是
A.称量前先调节托盘天平的零点
B.称量时左盘放被称量物,右盘放砝码
C.腐蚀性药品必须放在玻璃器皿里称量,其他药品可直接放在天平托盘上称量
D.用托盘天平可以准确称量至0.01g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com