
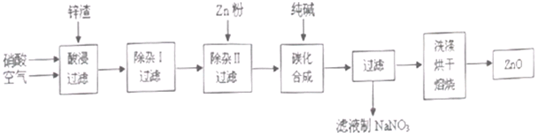
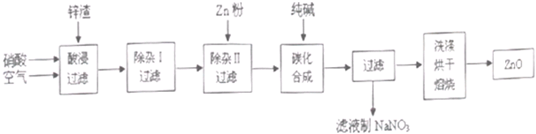
现从锌制品加工企业回收的废渣(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质)来制取氧化锌,流程如下:

有关氢氧化物完全沉淀的pH见下表:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
pH |
5.2 |
3.2 |
9.7 |
6.7 |
8.0 |
(l)在酸浸过程中,要提高锌元素的浸出率,可以采取 措施。
(2)上述流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
(3)在“除杂I”步骤中,将溶液调至pH=4的目的是 。在“除杂II”后,溶液的pH约为6,则此步过滤时滤渣中含有 。
(4)在“碳化合成”中,生成的产物之一为碱式碳酸锌[Zn2(OH)2CO3],同时放出CO2,请写出该反应的化学方程式 。
(5)从滤液中提取NaNO3晶体的操作步骤为 。
(6)在实验室如何洗涤过滤出的碱式碳酸锌? 。
(16分)
(1)加热、搅拌(2分)
(2)烧杯、玻璃棒、漏斗 (3分)
(3)使Fe3+转化为Fe(OH)3沉淀除去(2分)
Al(OH)3、Cu、Zn (2分) (不填Zn不扣分)
(4)2Na2CO3+2Zn(NO3)2+H2O=4NaNO3+Zn2(OH)2CO3+CO2↑(2分)
(5)蒸发浓缩、冷却结晶、过滤(3分)
(6)往漏斗中加入少量蒸馏水,浸没沉淀,让其自然滤出,反复几次(2分)
【解析】
试题分析:(1)增大反应物浓度、升高温度、增大压强(有气体参加的反应)、增大固体表面积、使用合适的催化剂、研磨、搅拌、振荡等措施,都是加快反应速率、提高浸出率的常用措施;(2)过滤分离固液混合物,常用的玻璃仪器有烧杯、普通漏斗、玻璃棒;(3)硝酸具有强氧化性和强酸性,酸性条件下空气中的氧气也能将亚铁离子氧化为铁离子,则溶液中含有Zn2+、Fe3+、Cu2+、Al3+、H+、NO3-,读表中信息可知,将溶液pH调至4时,铁离子完全变为氢氧化铁沉淀,可以除去溶液中的铁离子;将溶液pH调至6时,铝离子完全变为氢氧化铝沉淀,可以除去溶液中的铝离子,由于锌比铜活泼,则加入过量的锌不仅能消耗氢离子,而且能将铜离子完全还原为单质铜,既除去杂质,又没有引入新杂质,则除杂II所得滤渣主要成分为氢氧化铝、铜、锌;(4)依题意,加入的碳酸钠与硝酸锌溶液反应,生成碱式碳酸、二氧化碳,根据质量守恒原理可得该复分解反应方程式:2Na2CO3+2Zn(NO3)2+H2O=4NaNO3+Zn2(OH)2CO3+CO2↑;(5)硝酸钠是可溶性盐,溶解度随温度下降而明显减小,根据其性质推断,将滤液蒸发浓缩、冷却结晶、过滤得到硝酸钠晶体;(6)根据过滤之后洗涤沉淀的一般原理,洗涤碱式碳酸锌时,先向漏斗中加入少量蒸馏水,浸没沉淀,再让其自然滤出,反复几次即可。
考点:考查有关物质制备的化学工艺流程,涉及加快反应速率的措施、过滤、解释溶液pH控制到一定值的目的、滤渣成分、关键步骤的化学反应方程式、提取晶体的方法、沉淀的洗涤等。


科目:高中化学 来源: 题型:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 沉淀物 | AI(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:珠海一模 题型:问答题
| 沉淀物 | AI(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源:2013年广东省珠海市高考化学一模试卷(解析版) 题型:解答题

| 沉淀物 | AI(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com