
【题目】A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为易挥发液体,C为气体。
D、E、F、G、X均为化合物,其中X是一种无氧强酸、E为黑色固体,H在常温下为液体.它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
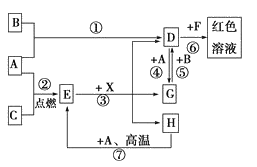
(1)写出化学式:A___,D___,E___,X___。
(2)在反应①~⑦中,不属于氧化还原反应的是____。(填编号)
(3)反应⑥的离子方程式为____。
(4)反应⑦的化学方程式为____。
(5)该反应中每消耗0.3mol的A,可转移电子___mol。
【答案】Fe Fe(NO3)3 Fe3O4 HCl ③⑥ Fe3++ 3SCN-![]() Fe(SCN)3 3Fe + 4H2O(g)
Fe(SCN)3 3Fe + 4H2O(g) ![]() Fe3O4 + 4H2 0.8
Fe3O4 + 4H2 0.8
【解析】
根据D加F为红色溶液,想到KSCN和铁离子显红色,再联想D到G的转化,是亚铁离子和铁离子之间的转化,故D为铁离子,G为亚铁离子,A为单质铁,而B和A要反应生成铁离子,再联系A为有液体且易挥发,说明是硝酸,再根据E和X反应生成D、G、H,说明E中有铁的两个价态, E为黑色固体,且Fe和C点燃变为黑色固体,想到E为四氧化三铁,X为盐酸,H为水。
⑴根据前面分析得出化学式:A:Fe,D:Fe(NO3)3,E:Fe3O4,X:HCl,故答案分别为Fe;Fe(NO3)3;Fe3O4;HCl;
⑵在反应①~⑦中,①~⑦反应分别属于①氧化还原反应,②氧化还原反应,③复分解反应,④氧化还原反应,⑤氧化还原反应,⑥复分解反应,⑦氧化还原反应,故不属于氧化还原反应的是③⑥,故答案为③⑥;
⑶反应⑥的离子方程式为Fe3++ 3SCN-![]() Fe(SCN)3,故答案为Fe3++ 3SCN-
Fe(SCN)3,故答案为Fe3++ 3SCN-![]() Fe(SCN)3;
Fe(SCN)3;
⑷反应⑦的化学方程式为3Fe + 4H2O(g) ![]() Fe3O4 + 4H2,故答案为3Fe + 4H2O(g)
Fe3O4 + 4H2,故答案为3Fe + 4H2O(g) ![]() Fe3O4 + 4H2;
Fe3O4 + 4H2;
⑸反应⑦中,铁化合价升高,水中氢化合价降低,分析氢总共降低了8个价态即转移8mol电子,因此每消耗0.3mol的A,可转移电子0.8 mol,故答案为0.8 mol。


科目:高中化学 来源: 题型:
【题目】如下图所示是某品牌饮用矿泉水标签的部分内容。

请认真阅读标签内容,计算:
(1)镁离子的物质的量浓度的最大值_______。
(2)一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过多少_______?(单位:mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 、
、![]() 、
、![]() 是三种原子序数依次增大的短周期元素。甲、乙、丙分别是三种元素形成的单质,
是三种原子序数依次增大的短周期元素。甲、乙、丙分别是三种元素形成的单质,![]() 、
、![]() 、
、![]() 、
、![]() 分别是由
分别是由![]() 、
、![]() 、
、![]() 形成的二元化合物,且
形成的二元化合物,且![]() 与
与![]() 分子中均含有10个电子。它们之间转化关系如图所示。下列说法正确的是( )。
分子中均含有10个电子。它们之间转化关系如图所示。下列说法正确的是( )。
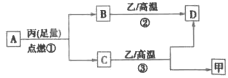
A.原子半径:![]()
B.![]() 与
与![]() 形成的化合物只含极性键
形成的化合物只含极性键
C.![]() 有多种同素异形体,且均具有高熔点、高沸点、硬度大的性质
有多种同素异形体,且均具有高熔点、高沸点、硬度大的性质
D.稳定性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃甲酸俗称糠酸,广泛应用于塑料工业、食品行业、涂料、医药、香料等。用呋喃甲醛制备呋喃甲酸和副产品呋喃甲醇的原理为:
反应1:![]() +NaOH
+NaOH![]()
![]() △H<0
△H<0
反应2:![]() +HCl
+HCl![]()
![]() +HCl
+HCl
某研究性学习小组利用上图装置制备呋喃甲酸的实验流程如下:
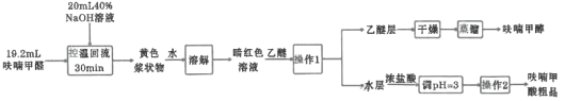
已知:①乙醚(![]() )沸点34.6℃,其蒸气有毒,可使人失去知觉。
)沸点34.6℃,其蒸气有毒,可使人失去知觉。
②主要试剂相关物理性质如下:
试剂 | 相对分子质量 | 密度/ | 熔点/℃ | 沸点/℃ | 溶解性 |
呋喃甲醛 | 96 | 1.16 |
| 161.7 | 微溶于水,易溶于乙醇、乙醚。 |
呋喃甲醇 | 98 | 1.13 |
| 171.0 | 溶于水,可混溶于乙醇、乙醚。 |
呋喃甲酸 | 112 | - | 129.5 | 231.0 | 微溶于冷水,在热水中溶解度较大,易溶于乙醇、乙醚。 |
请回答下列问题:
(1)“控温回流”时需控制反应温度8~12℃,应采取的控温方式是________,三颈烧瓶中所加入的![]() 溶液应如何预处理________,滴加呋喃甲醛时需________。
溶液应如何预处理________,滴加呋喃甲醛时需________。
(2)在“控温回流”时充分搅拌才能获得较高产率。其原因是________。
(3)“操作1”的名称为________,所用到的玻璃仪器主要有________,“操作2”主要包括________、________。
(4)“蒸馏”时,用下图________(填字母标号)装置更好,与另一装置相比,该装置的优点有①________;②________。
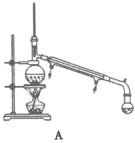
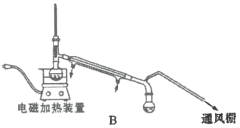
(5)呋喃甲酸粗品精制所采用的方法是________,最终得到精产品9.86g,呋喃甲酸的产率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有物质的量浓度均为0.1mo/L的下列溶液:
(1)①NH3·H2O ②FeCl2 ③NaHSO4 ④KOH ⑤Ba(OH)2 ⑥H2SO4,其pH由大到小的顺序排列的是(填序号)___。
(2)写出氯化亚铁溶液中,亚铁离子水解的离子方程式___。
(3)写出硫酸氢钠与氢氧化钡2:1反应的离子方程式___。
(4)将氢氧化钾与氯化亚铁溶液混合,现象___。依次发生的化学方程式____、___。
(5)氯化亚铁保存时为何加少量铁粉___,若保存硫酸铁溶液时应向溶液中加入____。
(6)如何利用氯水和硫氰化钾检验氯化亚铁溶液中的Fe2+,写出加入试剂的先后顺序和对应现象__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )

A. Mg比Al活泼,Mg失去电子被氧化成Mg2+
B. 铝条表面虽有氧化膜,但可不必处理
C. 该电池的内外电路中,电流均是由电子定向移动形成的
D. Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前铬被广泛应用于冶金、化工、铸铁及高精端科技等领域。回答下列问题:
(1)基态Cr原子价层电子的轨道表达式为_______,其核外有_______种不同能量的电子。
(2)Cr的第二电能离(ICr)和Mn的第二电离能(IMn)分别为1590.6 kJ·mol-1、1509.0 kJ·mol-1,ICr > IMn的原因是____________。
(3)过氧化铬CrO5中Cr的化合价为+6,则该分子中![]() 键、
键、![]() 键的数目之比为______。
键的数目之比为______。
(4)CrCl3的熔点(83℃)比CrF3的熔点(1100℃)低得多,这是因为___________。
(5)Cr的一种配合物结构如图所示,该配合物中碳原子的杂化方式是_______,阳离子中Cr原子的配位数为_________,ClO![]() 的立体构型为________。
的立体构型为________。

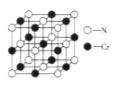
(6)氮化铬晶体的晶胞结构如图所示,Cr处在N所围成的________空隙中,如果N与Cr核间距离为apm,则氮化铬的密度计算式为__________g·cm-3(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二酸(![]() )俗称草酸,在实验研究和化学工业中应用广泛。完成下列填空:
)俗称草酸,在实验研究和化学工业中应用广泛。完成下列填空:
(1)室温下,测得![]() 溶液的
溶液的![]() ,写出草酸的电离方程式______。
,写出草酸的电离方程式______。
(2)草酸溶液中微粒的物质的量分数随溶液![]() 变化如图所示:
变化如图所示:
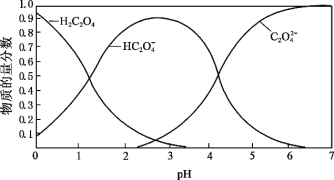
i.向草酸溶液中滴加![]() 溶液至
溶液至![]() 时发生的主要反应的离子方程式是:_______。
时发生的主要反应的离子方程式是:_______。
ii.继续加入![]() ,调节
,调节![]() 由2.5直至大于6.5,调节过程中
由2.5直至大于6.5,调节过程中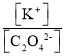 比值将________(选填“增大”、“减小”或“不变”)。
比值将________(选填“增大”、“减小”或“不变”)。
(3)工业上制取草酸的原理为:![]()
该反应的平衡常数表达式![]() _______,下列能说明反应已经达到平衡的是______。
_______,下列能说明反应已经达到平衡的是______。
a 平衡常数K保持不变 b 反应液的pH保持不变
c 丁醇的浓度保持不变 d 反应液的总质量保持不变
(4)草酸可用于测定高锰酸钾的质量分数,原理如下:![]()
i.一定条件下,测得上述反应中溶液中![]() 的浓度随反应时间的变化如图,以
的浓度随反应时间的变化如图,以![]() 浓度的变化表示此反应
浓度的变化表示此反应![]() 内的平均反应速率为____________
内的平均反应速率为____________![]()
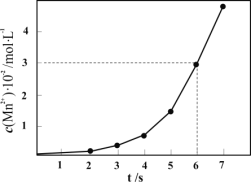
ii.分析![]() 的浓度随反应时间的变化的可能原因(反应过程中温度没有明显变化)_____。
的浓度随反应时间的变化的可能原因(反应过程中温度没有明显变化)_____。
(5)取![]() 的高锰酸钾产品,配成
的高锰酸钾产品,配成![]() 溶液,取出
溶液,取出![]() ,消耗
,消耗![]() 草酸标准溶液
草酸标准溶液![]() ,则样品中高锰酸钾的质量分数为______。
,则样品中高锰酸钾的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷是重要的气体燃料和化工原料。回答下列问题:
(1)已知![]() 、
、![]() 、
、![]() 的燃烧热分别为
的燃烧热分别为![]() ,
,![]() ,
,![]() 。利用甲烷制备合成气的反应为
。利用甲烷制备合成气的反应为![]()
![]() 。
。
根据上述数据能否计算![]() ________(填“能”或“否”),理由是________________。
________(填“能”或“否”),理由是________________。
(2)在某密闭容器中通入![]()
![]() 和
和![]() ,在不同条件下发生反应:
,在不同条件下发生反应:
![]()
![]()
测得平衡时![]() 的体积分数与温度、压强的关系如图所示。
的体积分数与温度、压强的关系如图所示。
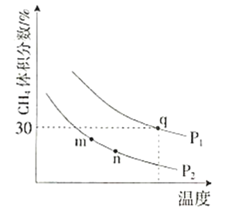
①![]() ________
________![]() ,
,![]() ________(填“<”、“>”或“=”)。
________(填“<”、“>”或“=”)。
②m、n、q三点的化学平衡常数大小关系为________。
③q点甲烷的转化率为________,该条件下的化学平衡常数![]() ________(用含有
________(用含有![]() 的表达式表示,
的表达式表示,![]() 为以分压表示的平衡常数)。
为以分压表示的平衡常数)。
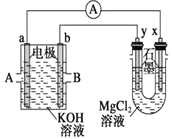
(3)用甲烷和![]() 构成的燃料电池电解
构成的燃料电池电解![]() 溶液,装置如下图所示。反应开始后,观察到x电极附近出现白色沉淀。则A处通入的气体是
溶液,装置如下图所示。反应开始后,观察到x电极附近出现白色沉淀。则A处通入的气体是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com