
| A. | NaCl | B. | MgCl2 | C. | NaHCO3 | D. | H2CO3 |
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:解答题
| 元素编号 | A | B | C | D | E | F | G | H | I |
| 原子半径/nm | 0.037 | 0.071 | 0.074 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高或最 低化合价 | +1 | -1 | -2 | -3 | +3 | -2 | +3 | +1 | +1 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某工艺原理示意图如下.其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2.
某工艺原理示意图如下.其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | Na2SO4溶液 | C. | 溴水 | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | 氢氧化铜溶液与硫酸反应:OH-+H+═H2O | |
| C. | 二氧化硅与氢氧化钠溶液反应:SiO2+2OH-═H2SiO3 | |
| D. | 碳酸钙与醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度,可提高反应速率 | |
| B. | 加入合适的催化剂,可提高N2的转化率 | |
| C. | N2的正反应速率等于NH3的逆反应速率 | |
| D. | 反应物和生成物的浓度都不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 序号 | 固体成分(填化学式) |
| 1 | |
| 2 | |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
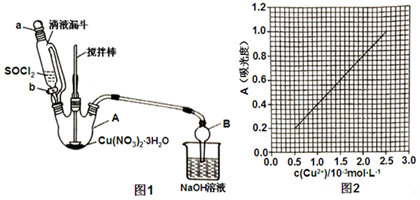
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.下列说法不正确的是( )
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.下列说法不正确的是( )| A. | a点反应的离子方程式为 IO3-+3HSO3-=I-+3SO42-+3H+ | |
| B. | b点到c点反应的离子方程式为 IO3-+5I-+6H+=3I2+3H2O | |
| C. | 当溶液中的I-为0.4 mol时,加入的KIO3只能为0.4 mol | |
| D. | 若往100 mL 1mol/L的KIO3溶液中逐滴滴加NaHSO3溶液,反应开始时的离子方程式为 2IO3-+5HSO3-=I2+5SO42-+H2O+3H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com