
��0��1mol��LһCH3COOH��Һ�д������µ���ƽ�⣺CH3COOH![]() CH3COOһ+H+�����ڸ�ƽ�⣬������������ȷ���� ( )
CH3COOһ+H+�����ڸ�ƽ�⣬������������ȷ���� ( )
A������ˮʱ��ƽ��������Ӧ�����ƶ�����Һ��n(H+)����
B���������������ᣬƽ��������Ӧ�����ƶ�����Һ��c(H+)����
C����������0��1 mol��L-HCl��Һ��ƽ�����淴Ӧ�����ƶ�����Һ��c(H+)��С
D����������CH3COONa���壬ƽ�����淴Ӧ�����ƶ�����Һ��c(H+)��С

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(10��)��֪25��ʱ����������ʵĵ���ƽ�ⳣ���������±���
�ش��������⣺
(1)���ʵ���Ũ�Ⱦ�Ϊ0��1mol��Lһ1��������Һ��a��CH3COONa b��Na2CO3 c��NaClO
d��NaHCO3��
pH��С���������˳����_______________________(����ĸ��ʾ)
(2)�����£�0��1mol��L��1��CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�����_______________(�����)
A��c��H+�� B��c(H+)��c(CH3COOH)
C��c(H+)��c(OH��) D��c(OH-)��c(H+)
(3)�����Ϊl00mL pH=2��CH3COOH��һԪ��HX����ˮϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��___________(����ڡ�����С�ڡ����ڡ�)CH3COOH�ĵ���ƽ�ⳣ���������ǣ�______________________________________��
(4)25��ʱ����CH3COOH��CH3COONa�Ļ����Һ�У������pH=6������Һ��
c(CH3COO��)��c(Na+)=_______mol��L��1(�ȷֵ)��c(CH3COO-)��c(CH3COOH)=_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��0.1mol/L Na2CO3��Һ�� ������ԡ��������ԡ������ԡ�������ԭ���� �������ӷ���ʽ��ʾ��
��2������ȼ�ϵ�����������ܵ�һ����Ҫ��ʽ����д������ȼ�ϵ�أ��������ҺΪKOH��Һ���ĸ����ĵ缫��Ӧʽ ��
��3��ij�¶��µ�ˮ��Һ�У�c��H+����10��xmol/L��
c��OH������10��y mol/L��x��y�Ĺ�ϵ����ͼ��ʾ��
���¶���ˮ�����ӻ�Ϊ���������� �������¶���0.01 mol/L NaOH��Һ��pHΪ������������
��4������ͼװ�ã���֪���缫�Ϸ����ĵ缫��Ӧ�ֱ�Ϊ��a����Cu2����2e����Cu
b����Fe��2e���� Fe2��
��װ����ԭ�������Һһ������ ������ţ�
A�� Cu2�� B��Na�� C��Fe2�� D�� Ag��
��5�����ᱵ��ˮ�д��ڳ����ܽ�ƽ�⣺BaSO4��s��Ba 2+ (aq)+ SO42��(aq) 25�� ʱ��BaSO4��Ksp=1.1��l0��10,��0.1 mol��Lһ1������Һ�У������ӵ�Ũ�����ɴﵽ mol��Lһ1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭���������ѧ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��1��0.1mol/L Na2CO3��Һ�� ������ԡ��������ԡ������ԡ�������ԭ���� �������ӷ���ʽ��ʾ��
��2������ȼ�ϵ�����������ܵ�һ����Ҫ��ʽ����д������ȼ�ϵ�أ��������ҺΪKOH��Һ���ĸ����ĵ缫��Ӧʽ ��
��3��ij�¶��µ�ˮ��Һ�У�c��H+����10��xmol/L��c��OH������10��y mol/L��x��y�Ĺ�ϵ��ͼ��ʾ�����¶���ˮ�����ӻ�Ϊ �����¶���0.01 mol/L NaOH��Һ��pHΪ ��
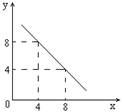
��4����ͼװ�ã���֪���缫�Ϸ����ĵ缫��Ӧ�ֱ�Ϊ��
a����Cu2����2e���� Cu b����Fe��2e���� Fe2��
��װ����ԭ�������Һһ������ ��������ţ�
A�� Cu2�� B��Na�� C��Fe2�� D�� Ag��
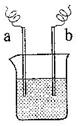
��5�����ᱵ��ˮ�д��ڳ����ܽ�ƽ�⣺BaSO4��s��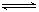 Ba2+ (aq)+ SO42��(aq) 25��ʱ��BaSO4��Ksp=1.1��l0��10,��0.1 mol��Lһ1������Һ�У������ӵ�Ũ�����ɴﵽ mol��Lһ1��
Ba2+ (aq)+ SO42��(aq) 25��ʱ��BaSO4��Ksp=1.1��l0��10,��0.1 mol��Lһ1������Һ�У������ӵ�Ũ�����ɴﵽ mol��Lһ1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��1��0.1mol/L Na2CO3��Һ�� ������ԡ��������ԡ������ԡ�������ԭ���� �������ӷ���ʽ��ʾ��
��2������ȼ�ϵ�����������ܵ�һ����Ҫ��ʽ����д������ȼ�ϵ�أ��������ҺΪKOH��Һ���ĸ����ĵ缫��Ӧʽ ��
��3��ij�¶��µ�ˮ��Һ�У�c��H+����10��xmol/L��
c��OH������10��y mol/L��x��y�Ĺ�ϵ����ͼ��ʾ��

���¶���ˮ�����ӻ�Ϊ���������� �������¶���0.01 mol/L NaOH��Һ��pHΪ������������
��4������ͼװ�ã���֪���缫�Ϸ����ĵ缫��Ӧ�ֱ�Ϊ��a����Cu2����2e���� Cu
b����Fe��2e���� Fe2��
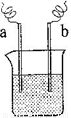
��װ����ԭ�������Һһ������ ������ţ�
A�� Cu2�� B��Na�� C��Fe2�� D�� Ag��
��5�����ᱵ��ˮ�д��ڳ����ܽ�ƽ�⣺BaSO4��s��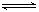 Ba 2+ (aq)+ SO42��(aq) 25��
ʱ��BaSO4��Ksp=1.1��l0��10,��0.1 mol��Lһ1������Һ�У������ӵ�Ũ�����ɴﵽ
mol��Lһ1
Ba 2+ (aq)+ SO42��(aq) 25��
ʱ��BaSO4��Ksp=1.1��l0��10,��0.1 mol��Lһ1������Һ�У������ӵ�Ũ�����ɴﵽ
mol��Lһ1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com