
|
在10 ml 0.1 mol/L NaOH溶液中加入等体积、等浓度的CH3COOH溶液,反应后溶液中各粒子的浓度关系错误的是 | |
A. |
C(Na+)>C(CH3COO-)>C(H+)>C(OH-) |
B. |
C(Na+)>C(CH3COO-)>C(OH-)>C(H+) |
C. |
C(Na+)=C(CH3COO-)+C(CH3COOH) |
D. |
C(Na+)+C(H+)=C(CH3COO-)+C(OH-) |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:学习高手选修化学(反应原理人教版) 人教版 题型:013
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氯化铵溶液呈酸性 NH |
B. |
氢硫酸电离 H2S |
C. |
向小苏打溶液中加入醋酸溶液 HCO |
D. |
在标准状况下,向10 mL 0.1 mol·L-1 FeBr2溶液中通入22.4 mL Cl2 2Fe2++2Br-+2Cl2 |
查看答案和解析>>
科目:高中化学 来源:天津市蓟县一中2011-2012学年高二上学期第三次月考化学试题 题型:013
|
在相同的温度时100 mL 0.01 mol·L-1的醋酸溶液与10 mL 0.1 mol·L-1醋酸溶液相比较,下列数值前者大于后者的是 | |
| [ ] | |
A. |
中和时所需氢氧化钠的物质的量 |
B. |
H+浓度 |
C. |
H+的物质的量 |
D. |
CH3COOH的物质的量 |
查看答案和解析>>
科目:高中化学 来源:志鸿系列训练必修一化学鲁科版 题型:013
|
在10 mL 0.1 mol·L-1 H2SO4溶液中逐滴加入0.1 mol·L-1 Ba(OH)2溶液至过量,溶液的导电能力将 | |
| [ ] | |
A. |
逐渐减小 |
B. |
逐渐增大 |
C. |
不变 |
D. |
先减小后增大 |
查看答案和解析>>
科目:高中化学 来源:江苏省扬州中学2012届高三3月双周练习(一)化学试题 题型:058
钇(Y)元素常见化合价为+3是激光和超导的重要材料.我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),以此矿石为原料生产氧化钇(Y2O3)的主要流程如下:
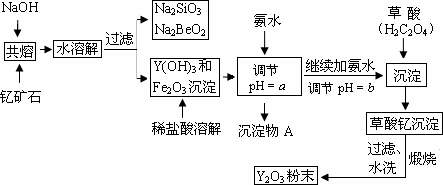
已知:①有关金属离子形成氢氧化物沉淀时的pH如下表:
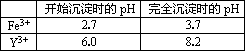
②在周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似.
(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为________.
(2)欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀.则
①最好选用盐酸、________(填字母)两种试剂,再通过必要的操作即可实现.
a.NaOH溶液
b.氨水
c.CO2气
d.HNO3
②写出Na2BeO2与足量盐酸发生反应的离子方程式:________.
(3)检验草酸钇沉淀是否洗涤干净的操作方法是________.
(4)10 mL 0.1 mol/L H2C2O4溶液与10 mL 0.1 mol/L NaOH溶液混合后溶液显酸性,溶液中离子浓度由大到小的排列顺序是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com