
| A、K、Na、Al |
| B、F、O、N |
| C、As、P、H |
| D、Se、S、O |


科目:高中化学 来源: 题型:
 某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)
某化学兴趣小组用电解CuSO4溶液的方法,测定铜的相对原子质量.(装置如图所示)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
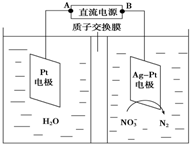 目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )
目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为NO3- 或NO2-,然后再用电解的方法除去NO3-和NO2-,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是( )| A、Pt电极为阴极 |
| B、电解过程中H+向正极移动 |
| C、理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5 |
| D、电解过程中Pt电极附近溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.
某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鉴别食盐和纯碱 |
| B、验证蛋壳的主要成分为CaCO3 |
| C、除去热水瓶内壁上的水垢 |
| D、检验自来水中是否含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验鸡蛋壳中含有碳酸盐 |
| B、检验蛋白质在加热条件下能发生变性 |
| C、检验加碘食盐中不含碘单质 |
| D、检验自来水中含有Cl-离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com