
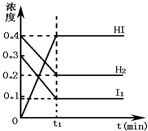
 可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答:
可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答:| △c |
| △t |
| 转化了的浓度 |
| 起始浓度 |
| 0.2 |
| t1 |
| 0.2 |
| t1 |
| 转化了的浓度 |
| 起始浓度 |
| 0.3-0.1 |
| 0.3 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑧ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
| 4 | ② | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B两种固体物质的溶解度曲线如图所示.请回答:
A、B两种固体物质的溶解度曲线如图所示.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
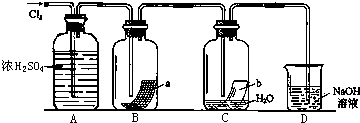 为验证干燥的Cl2没有漂白性,而Cl2与水反应后的产物具有漂白性,肖飞同学设计了如下实验.(其中a是有色布条)
为验证干燥的Cl2没有漂白性,而Cl2与水反应后的产物具有漂白性,肖飞同学设计了如下实验.(其中a是有色布条)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃,NaHCO3在水中的溶解度比Na2CO3的小 |
| B、Na2O和Na2O2中的阴阳离子个数比不相等 |
| C、用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色说明原溶液中有Na+无K+ |
| D、Na与足量O2反应,随温度升高生成Na2O的速率逐渐加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO2的水解产物是Ca(OH)2和H2O2 |
| B、PCl3的水解产物是PH3和HClO |
| C、NaClO的水解产物之一是HClO |
| D、Mg3N2与足量盐酸反应的产物是NH4Cl和MgCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com