
有①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25 mL,物质的量浓度均为0.1 mol/L,下列说法正确的是( )
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol·L-1的盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
科目:高中化学 来源: 题型:
硫元素有多种化合价,可形成多种化合物。
(1)旋转喷雾干燥法是去除燃煤烟气中二氧化硫的方法之一,工艺流程如下图所示,写出雾化器中发生反应的化学方程式:________________________________________________。
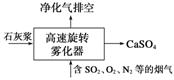
(2)已知NaHSO3溶液显弱酸性,其原因用离子方程式表示为____________。
(3)请按照浓度由大到小的顺序排列0.1 mol·L-1 Na2SO3 溶液中的离子________。Na2SO3溶液放置于空气中一段时间后,溶液的pH________(填“增大”、“减小”或“不变”)。
(4)某同学在常温下设计如下实验流程探究Na2S2O3的化学性质。
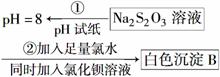
实验①可说明________(填字母)。
A.该Na2S2O3溶液中水电离的c(OH-)=10-8 mol·L-1
B.H2S2O3是一种弱酸
C.Na2S2O3是一种弱电解质
D.Na2S2O3能发生水解,其离子方程式为S2O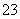 +2H2O===H2S2O3+2OH-
+2H2O===H2S2O3+2OH-
实验②说明Na2S2O3具有________性。写出发生反应的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Li3N中氮以N3-存在,基态N3-的电子排布式为________。
(2)O=O键的键能为497.3kJ·mol-1,O—O键的键能为142kJ·mol-1,说明O2中的________键更稳定(填“σ”或“π”)。
(3)BF3与F-可形成BF4-离子。BF3与F-形成BF4-离子时,二者形成的化学键为________键。
(4)X+中所有电子正好充满K、L、M三个电子层,则X的元素符号是________,基态X+的电子排布式为_____________________________________________。
(5)与N2互为等电子体的一种分子为 (填化学式),该分子中σ键与π键的个数比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器内,发生如下反应N2+3H2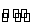 2NH3。
2NH3。
(1)若反应到某时刻t时,n(N2)=13 mol, n(NH3)=6 mol,a=_______。
(2)反应到达平衡时,混合气体体积为716.8 L(标准状况)其中NH3的含量(体积分数)为25%,计算平衡时NH3的物质的量_________。
(3)混合气体中a∶b=_________。
(4)平衡混合气体中n(N2)∶n(H2)∶n(NH3)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、NaHSO4溶液和BaCl2溶液中的一种,已知A、B溶液的pH相同,A、C混合后溶液变浑浊。下列说法正确的是( )
A.D溶液的pH<7 B.C溶液中的溶质溶于水促进了水的电离
C.溶液A滴入到碳酸氢钠溶液中产生气体 D.溶液B进行焰色反应呈黄色
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组在实验室中利用CaSO4、NH3、CO2制备(NH4)2SO4,工艺流程如下。
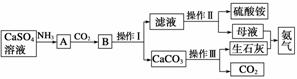
回答下列问题:
(1)操作Ⅰ的名称________,操作Ⅱ需要用到的仪器有铁架台(带铁圈)、酒精灯、玻璃棒和________。
(2)所得母液显酸性的原因用离子方程式表示为______________。检验该溶液含有铵根离子的方法是____________________________。
(3)下列装置能用于实验室制氨气的是________(填序号)。
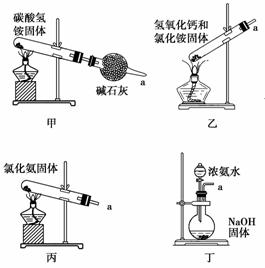
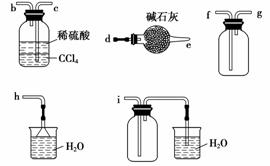
选择氨气的制取装置后,再选用下列装置收集干燥的氨气,并制取硫酸铵溶液,连接的顺序(用接口序号字母表示)是:a接__________________________。
(4)该小组还通过实验研究氨气的性质。
利用下图所示装置探究NH3能否被NO2氧化(K1、K2为止水夹,夹持固定装置略去)。
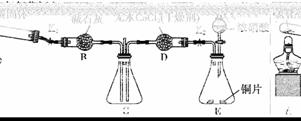
E装置中制取NO2反应的离子方程式是____________。A中发生反应的化学方程式为__________________。
若NH3能被NO2氧化全部生成无毒物质,预期观察到C装置中的现象是____________。若此反应转移电子0.4 mol,则消耗标准状况下的NO2________ L。
实验过程中,未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
①NO2氧化性较弱,不能将NH3氧化;
②在此条件下,NH3的转化率极低;
③________________________________________________________________________。
此实验装置存在一个明显的缺陷是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组的同学通过对亚硫酸钠组成元素的价态进行分析后认为Na2SO3溶液在存放过程中有可能变质,若已变质,则相应反应的化学方程式为__________________________。
(1)甲同学设计了如下两种方案来检验Na2SO3溶液是否变质。
方案Ⅰ:取样,加入稀盐酸有气泡生成,认为Na2SO3溶液没有变质。
方案Ⅱ:取样,加入氯化钡溶液有白色沉淀生成,认为Na2SO3溶液完全变质。
乙同学认为上述两种方案均不合理,乙同学作出判断的依据分别是方案Ⅰ:________;方案Ⅱ:________。
(2)乙同学设计如图所示装置(夹持装置已略去)探究Na2SO3溶液是否变质,量取60 mL标签上注明为1.0 mol·L-1的Na2SO3溶液放入A装置中,通过测量生成的SO2质量的方法来判断其是否变质。
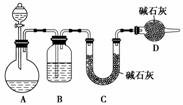
①D装置的作用是________,该实验装置中还存在一个明显的缺陷是________________,分液漏斗中应加入足量的________(填字母);
a.浓硝酸 b.65%硫酸
c.浓盐酸 d.20%硫酸
②改进缺陷后再进行实验,若实验前后测得C装置增重3.2 g,则Na2SO3变质的百分率是__________。
(3)丙同学认为若只是确定Na2SO3是否变质,乙的方案太复杂了,他认为只需要试管、胶头滴管、盐酸及氯化钡溶液就可以达到目的(不考虑对环境的影响),请你发表自己的看法(若不同意,请说明理由;若同意,请写出主要操作、现象及结论):______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确且能达到预期目的的是( )
| 实验目的 | 操作 | |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 欲证明CH2===CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫色是否褪去 |
| ③ | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| ④ | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
| ⑤ | 比较铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| ⑥ | 比较碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO2水溶液的pH |
A.①④⑤ B.②③⑤
C.①⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com