
| A. | 正丁烷的结构简式:C4H10 | |
| B. | S2-的结构示意图: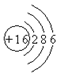 | |
| C. | NH3的电子式: | |
| D. | 碳酸钠电离方程式:Na2CO3=Na++CO32- |
分析 A.C4H10为正丁烷的分子式,不是结构简式;
B.硫离子的核外电子总数为18,最外层达到8电子稳定结构;
C.氨气为共价化合物,分子中含有3个N-H键;
D.电离方程式两边正电荷不相等,违反了电荷守恒.
解答 解:A.正丁烷的碳原子不能合并,其正确的结构简式为:CH3CH2CH2CH3,故A错误;
B.S2-的核电荷数为16,核外电子总数为18,其正确的离子结构示意图为: ,故B错误;
,故B错误;
C.NH3为共价化合物,N原子最外层达到8电子稳定结构,其电子式为: ,故C正确;
,故C正确;
D.碳酸钠为强电解质,在溶液中完全电离,其电离方程式为:Na2CO3=2Na++CO32-,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及结构简式、电子式、电离方程式、离子结构示意图等知识,明确常见化学用语的书写原则为解答关键,试题有利于提高学生的规范答题能力.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 10种 | C. | 12种 | D. | 16种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF+H2O?H3O++F- | |
| B. | NaHCO3=Na++HCO3-,HCO3-?H++CO32- | |
| C. | Ag2S(s)?2Ag+(aq)+S2-(aq) | |
| D. | S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,1 mol•L-1氨水与0.5 mol•L-1氨水中c(OH-)之比是2:1 | |
| B. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)═2c(H+)+c(CH3COOH) | |
| C. | 向0.2 mol•L-1 NaHCO3溶液中加入等体积0.1 mol•L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | CH3COOH是弱电解质,NH3•H2O是弱电解质,故CH3COONH4也是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入催化剂,改变了反应的途径,加快了反应速率,反应的△H也之改变 | |
| B. | 改变压强,反应速率发生改变,但平衡不发生移动,反应放出的热量不变 | |
| C. | 温度降低,正、逆反应速率都减小,反应放出的热量不变 | |
| D. | 恒容时充入稀有气体或充入H2,正、逆反应速率都减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
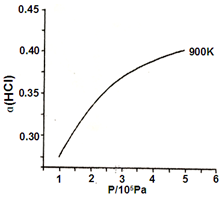 氯及其化合物在生活和生产中应用广泛.
氯及其化合物在生活和生产中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
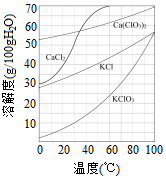 工业上制取氯酸钾的主要步骤为:
工业上制取氯酸钾的主要步骤为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | ⑦ | ③ | ||
| 实验结论 | ⑥ | ① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com