
| A、增重的4.4g为参加反应的CO2的质量 |
| B、溶质为Na2CO3 |
| C、溶质为NaHCO3 |
| D、低温蒸干溶液,所得固体的质量为:原溶液中NaOH的质量+4.4g |
| 4.4g |
| 44g/mol |


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
 实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )
实验室用0.10mol?L-1的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示,图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH,下列叙述不正确的是( )| A、此一元弱酸HA的电离平衡常数Ka≈1×10-4mol?L-1 |
| B、此弱酸的起始浓度约为1×10-2mol?L-1 |
| C、此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂 |
| D、当混合液pH=7时,溶液中c(HA)>c(A-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、在蒸馏烧瓶中盛约
| ||
| B、收集到的液体取少量滴入硝酸银和稀硝酸,无明显现象 | ||
| C、冷水从冷凝管下口进,上口出 | ||
| D、将温度计水银球插到蒸馏烧瓶内的自来水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
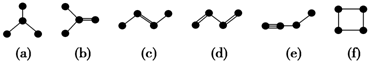
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于2V mL |
| B、小于2V mL |
| C、大于2V mL |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
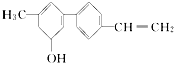 某有机化合物的结构简式如图所示:关于该化合物的下列说法正确的是( )
某有机化合物的结构简式如图所示:关于该化合物的下列说法正确的是( )| A、该有机物分子式C15H14 |
| B、完全燃烧时只有二氧化碳和水两种产物 |
| C、分子中苯环上连有羟基属于酚 |
| D、由于含有氧元素不是有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、绿色食品是不含任何化学物质的食品 |
| B、Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂 |
| C、与同浓度的硫酸反应时,NaHCO3比Na2CO3剧烈 |
| D、称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液,则放出氢气的体积(同温同压下)不相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com